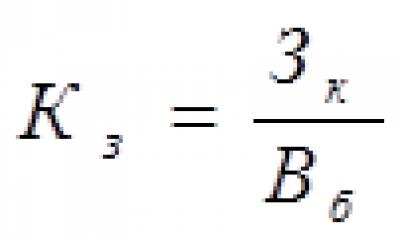ГОСТ 31694-2012
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ
Метод определения остаточного содержания антибиотиков тетрациклиновой группы с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Food products, food raw materials. Method of determination of the antibiotic residues of tetracycline group by High Performance Liquid Chromatography - Mass Spectrometry
МКС 67.050
67.100
Дата введения 2013-07-01
Предисловие
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением "Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов" (ФГБУ "ВГНКИ")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 1 октября 2012 г. N 51-2012)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Код страны по | Сокращенное наименование национального органа по стандартизации |
Минэкономики Республики Армения |
||
Беларусь | Госстандарт Республики Беларусь |
|
Казахстан | Госстандарт Республики Казахстан |
|
Кыргызстан | Кыргызстандарт |
|
Молдова-Стандарт |
||
Российская Федерация | Росстандарт |
|
Узбекистан | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. N 1424-ст межгосударственный стандарт ГОСТ 31694-2012 введен в действие в качестве национального стандарта Российской Федерации с 01 июля 2013 г.
5 Стандарт подготовлен на основе ГОСТ Р 53601-2009
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в ежемесячно издаваемом информационном указателе "Национальные стандарты".
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемом информационном указателях "Национальные стандарты". В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в ежемесячно издаваемом информационном указателе "Национальные стандарты"
ВНЕСЕНО Изменение N 1 , утвержденное и введенное в действие Приказом Федерального агентства по техническому регулированию и метрологии от 27 октября 2016 года N 1523-ст c 01.03.2017
Изменение N 1 внесено изготовителем базы данных по тексту ИУС N 2, 2017 год
ВНЕСЕНЫ: поправка , опубликованная в ИУС N 7, 2017 год; поправка , опубликованная в ИУС N 10, 2018 год
Поправки внесены изготовителем базы данных
1 Область применения
Настоящий стандарт устанавливает метод идентификации и количественного определения остаточного содержания антибиотиков тетрациклиновой группы в молоке, молочной продукции, яйцах, яичном порошке, меде, органах и тканях животных в продуктах переработки мясного сырья, мяса птицы, субпродуктах, в том числе птичьих, рыбе, нерыбных объектах и продукции из них с использованием высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием в диапазоне измерений от 1,0 до 1000,0 мкг/кг.
(Измененная редакция, Изм. N 1).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 * Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
________________
* На территории Российской Федерации действует ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
ГОСТ 12.2.085-2002 Сосуды, работающие под давлением. Клапаны предохранительные. Требования безопасности
ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 908-2004 Кислота лимонная моногидрат пищевая. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
ГОСТ ИСО 5725-6-2003** Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
________________
** На территории Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
ГОСТ 8981-78 Эфиры этиловый и нормальный бутиловый уксусной кислоты технические. Технические условия
ГОСТ 10652-73 Реактивы. Соль динатриевая этилендиамин-N, N, N", N"-тетрауксусной кислоты 2-водная (трилон Б). Технические условия
ГОСТ 13867-68 Продукты химические. Обозначения чистоты
ГОСТ 19792-2001 *** Мед натуральный. Технические условия
________________
*** На территории Российской Федерации действует ГОСТ Р 54644-2011 "Мед натуральный. Технические условия".
ГОСТ 24104-2001 **** Весы лабораторные. Общие технические требования
________________
**** На территории Российской Федерации действует ГОСТ Р 53228-2008 "Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания".
ГОСТ 26809.1-2014 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 1. Молоко, молочные, молочные составные и молокосодержащие продукты
ГОСТ 26809.2-2014 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 2. Масло из коровьего молока, спреды, сыры и сырные продукты, плавленые сыры и плавленые сырные продукты
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 29245-91 Консервы молочные. Методы определения физических и органолептических показателей
ГОСТ 31339-2006 Рыба, нерыбные объекты и продукция из них. Правила приемки и методы отбора проб
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
ГОСТ 31654-2012 Яйца куриные пищевые. Технические условия
ГОСТ 31720-2012 Пищевые продукты переработки яиц сельскохозяйственной птицы. Методы отбора проб и органолептического анализа"
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов по указателю "Национальные стандарты", составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
(Измененная редакция, Изм. N 1), (Поправка . ИУС N 10-2018).
3 Сущность метода
3.1 Определение остаточных количеств антибиотиков тетрациклиновой группы проводят методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (ВЭЖХ-МС/МС).
Метод ВЭЖХ-МС/МС обеспечивает хроматографическое разделение антибиотиков тетрациклиновой группы и их эпи-форм (приложение А).
3.2 Количественное определение остаточного содержания антибиотиков тетрациклиновой группы проводят методом внутреннего стандарта по сумме площадей пиков идентифицированных соединений и их эпи-форм для каждого антибиотика при помощи градуировочной кривой.
3.3 Детектирование анализируемых проб проводят в режиме регистрации выбранных реакций.
4 Средства измерений, вспомогательное оборудование, материалы, реактивы
4.1 При определении содержания антибиотиков тетрациклиновой группы применяют следующие средства измерений, вспомогательное оборудование и материалы:
- масс-спектрометр с диапазоном измерения от 100 до 500 атомных единиц массы (а.е.м.), массовым разрешением не менее 500, точностью измерения массы не ниже 0,2 а.е.м., с режимом получения и анализа фрагментных ионов (режим МС/МС);
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем; термостата хроматографической колонки, обеспечивающего температуру нагрева до 50°С;
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов масс-спектрометрических измерений;
- весы лабораторные по ГОСТ 24104 , высокого или специального класса точности, с наибольшим пределом взвешивания 200 и 500 г с ценой поверочного деления 0,1 и 1,0 мг соответственно;
- рН-метр с набором электродов, с пределами абсолютной погрешности измерений ±0,01 рН;
- пипетки одноканальные переменного объема 10-100 мм, 40-200 мм, 200-1000 мм, 1-5 см;
- пробирки мерные стеклянные П-1-5-0,1ХС, П-2-10-14/23 по ГОСТ 1770 ;
- пипетки стеклянные градуированные по ГОСТ 29227 ;
- колбы мерные стеклянные К-2-100-2, К-2-1000-2 по ГОСТ 1770 ;
- виалы (флаконы полипропиленовые) вместимостью 15 и 50 см с герметично закрывающимися пластмассовыми крышками ;
- фильтры мембранные с размером пор не более 0,5 мкм ;
- измельчитель-гомогенизатор лабораторный ;
- встряхиватель вибрационный для пробирок орбитального типа движения с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2500 об/мин ;
- центрифугу лабораторную рефрижераторную со скоростью вращения ротора не менее 10000 об/мин и диапазоном температур охлаждения от 4°С до 20°С, с адаптерами для пробирок вместимостью 15 см и микроцентрифужных пробирок вместимостью 1,5 см ;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования 40°С ;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм ;
- колонку хроматографическую обращенно-фазную длиной не менее 50 мм с диаметром частиц сорбента не более 5 мкм;
- устройство вакуумное для твердофазной экстракции;
- картридж для твердофазной экстракции объемом не менее 12 см, заполненный обращенно-фазным сорбентом с диаметром частиц не более 50 мкм;
- камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 18°С до минус 24°С;
- холодильник бытовой с морозильной камерой, цифровым контроллером температуры и рабочим диапазоном температур от 0°С до 5°С.
(Измененная редакция, Изм. N 1).
4.2 При определении содержания антибиотиков тетрациклиновой группы применяют следующие реактивы:
- кислоту лимонную пищевую по ГОСТ 908 , высшего сорта;
- метанол х.ч.;
- ацетонитрил ч.д.а.;
- деионизованную воду;
- муравьиную кислоту ч.д.а. по ГОСТ 5848 ;
- натрий фосфорнокислый двузамещенный дигидрат ч.д.а по ГОСТ 245 ;
- соль динатриевую этилендиаминтетрауксусной кислоты (трилон Б) по ГОСТ 10652 ;
- ортофосфорную кислоту по ГОСТ 6552 ;
- этилацетат по ГОСТ 8981 ;
- ацетон по ГОСТ 2603 ;
- стандартный образец тетрациклина гидрохлорида с содержанием действующего вещества не менее 90% ;
- стандартный образец окситетрациклина гидрохлорида с содержанием действующего вещества не менее 90% ;
- стандартный образец хлортетрациклина гидрохлорида с содержанием действующего вещества не менее 90% ;
- стандартный образец доксициклина с содержанием действующего вещества не менее 90% ;
- стандартный образец демеклоциклина с содержанием действующего вещества не менее 90% .
Все реактивы должны относиться к подгруппе чистоты 2 (х.ч.) или 3 (ч.д.а.) по ГОСТ 13867 .
5 Требования безопасности
5.1 Используемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007 , при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005 .
5.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
5.3 Операции по приготовлению и дозированию градуировочных растворов следует проводить под тягой в вытяжном шкафу.
5.4 В связи с тем, что при работе на хромато-масс-спектрометре используется сжатый азот, следует соблюдать требования ГОСТ 12.2.085 и правил устройства и безопасной эксплуатации сосудов, работающих под давлением, действующих на территории государства, принявшего стандарт.
5.5 При выполнении измерений на хромато-масс-спектрометре следует соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019 и инструкцией по эксплуатации прибора.
5.6 К выполнению измерений методом высокоэффективной жидкостной хроматографии - масс-спектрометрии допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации аппаратуры.
6 Порядок подготовки к проведению измерений
6.1 Отбор проб
6.1.1 Отбор проб проводят в соответствии с методическими указаниями по отбору проб пищевой продукции с целью лабораторного контроля качества и безопасности, утвержденными на территории государства, принявшего стандарт.
6.1.2 Отбор проб органов, тканей животных и птицы производят в соответствии с ГОСТ 31467 . Масса средней пробы органов, тканей животных и птицы не менее 200 г.
(Измененная редакция, Изм. N 1).
6.1.3 Отбор проб молока и молочных продуктов производят в соответствии с ГОСТ 26809.1 и ГОСТ 26809.2 . Объем средней пробы молока не менее 200 см, масса средней пробы образцов молочных продуктов не менее 250 г.
(Измененная редакция, Изм. N 1).
6.1.4 Отбор проб меда производят в соответствии с ГОСТ 19792 . Масса средней пробы меда не менее 200 г.
6.1.5 Отбор проб яиц и яичного порошка производят в соответствии с ГОСТ 31654 и ГОСТ 31720 . От яиц в качестве средней пробы отбирают не менее 12 шт.; масса средней пробы яичного порошка не менее 200 г.
(Измененная редакция, Изм. N 1).
6.1.6 Отбор проб рыбы, нерыбных объектов и продукции из них проводят по ГОСТ 31339 . Срок хранения отобранных проб при температуре от 2°С до 8°С - двое суток. При отсутствии возможности исследования проб в течение двух суток образцы должны быть заморожены при температуре минус 20°С на срок хранения не более 2 мес.
(Введен дополнительно, Изм. N 1).
6.2 Подготовка хромато-масс-спектрометрической системы к выполнению измерений
Подготовку хромато-масс-спектрометра к работе осуществляют в соответствии с техническим руководством по эксплуатации прибора.
При этом должны быть соблюдены следующие условия:
Температура окружающего воздуха | от 15°С до 30°С; |
Атмосферное давление | от 84 до 106 кПа; |
Относительная влажность воздуха | от 20% до 80%. |
(Поправка . ИУС N 7-2017).
6.3 Приготовление растворов
6.3.1 Приготовление раствора лимонной кислоты молярной концентрации 0,1 моль/дм
В мерную колбу вместимостью 1000 см вносят 21 г лимонной кислоты, растворяют в деионизированной воде и доводят объем до метки этим же растворителем.
6.3.2 Приготовление раствора гидрофосфата натрия молярной концентрации 0,2 моль/дм
В мерную колбу вместимостью 1000 см вносят 35,6 г двузамещенного фосфата натрия, растворяют в деионизированной воде и доводят объем до метки этим же растворителем.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.3 Приготовление буферного раствора
Для приготовления буферного раствора в мерной колбе вместимостью 1000 см смешивают в соотношении 60:40 растворы лимонной кислоты и гидрофосфата натрия, полученные по 6.3.1 и 6.3.2, добавляют 37,2 г трилона Б, измеряют рН и, при необходимости, доводят значение рН до 4,0 ортофосфорной кислотой.
(Измененная редакция, Изм. N 1).
6.3.4 Приготовление растворов элюентов мобильной фазы А и Б
6.3.4.1 Для приготовления раствора элюента мобильной фазы А в мерную колбу вместимостью 1000 см приливают деионизованную воду, добавляют 5 см муравьиной кислоты и доводят объем до метки деионизованной водой.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.4.2 Для приготовления раствора элюента мобильной фазы Б в мерную колбу вместимостью 1000 см приливают метиловый спирт, добавляют 5 см муравьиной кислоты и доводят объем до метки метиловым спиртом.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.5 Приготовление градуировочных растворов
6.3.5.1 Приготовление градуировочных растворов тетрациклинов
Для приготовления градуировочных растворов тетрациклинов на весах с наибольшим пределом взвешивания 500 г взвешивают по 10 мг каждого стандартного образца по 4.1 (кроме демеклоциклина) и переносят в мерную пробирку вместимостью 10 см. Добавляют метанол, помещают в ультразвуковую баню на 1 мин и доводят полученный раствор до метки метанолом.
Массовая концентрация каждого антибиотика тетрациклиновой группы в растворе составляет 1 мг/см.
6.3.5.2 Приготовление раствора демеклоциклина (внутреннего стандарта)
Для приготовления раствора внутреннего стандарта на весах с наибольшим пределом взвешивания 500 г взвешивают 10 мг стандарта демеклоциклина гидрохлорида и переносят в мерную пробирку вместимостью 10 см. Добавляют метанол, помещают в ультразвуковую баню на 1 мин, доводят полученный раствор до метки метанолом.
Массовая концентрация внутреннего стандарта в растворе составляет 1 мг/см. Путем нескольких разбавлений доводят массовую концентрацию раствора внутреннего стандарта до значения 1 мкг/см. Раствор с данной концентрацией используют для внесения в исследуемые образцы.
Срок хранения раствора - 3 мес при температуре минус 20°С.
Перед применением растворы выдерживают при комнатной температуре, в темном месте, не менее 20 мин.
6.4 Хроматографические условия измерений
6.4.1 Хромато-масс-спектрометр включают и настраивают в соответствии с техническим руководством по его эксплуатации и устанавливают следующие хроматографические параметры:
- скорость потока элюента - 200 мм/мин;
- объем вводимой пробы - 20 мм.
6.4.2 Детектирование пиков проводится методом "регистрации выбранных реакций". Для каждого антибиотика тетрациклиновой группы измеряется сигнал для двух фрагментных ионов согласно таблице 1.
_______________
"Регистрация выбранных реакций" - режим работы масс-спектрометра, при котором детектируется ионный ток только для выбранных фрагментных ионов выбранных ионов-прекурсоров.
Таблица 1 - Значения масс ионов-предшественников и ионов-фрагментов
Ион-предшественник, m/z* | Ионы-фрагменты, m/z* |
|
Тетрациклин | ||
Окситетрациклин | ||
Доксициклин | ||
Хлортетрациклин | ||
Демеклоциклин | ||
* m/z - отношение массы иона к его заряду. |
||
Более интенсивный пик (верхний в каждой строке таблицы 1) служит для определения концентрации антибиотика, второй (нижний в каждой строке таблицы 1) используется для подтверждения правильности определения. Пики ионов-фрагментов с массой 410,1 тетрациклина и доксициклина различаются по времени их удержания в хроматографической колонке, определяемому на стадии разработки ВЭЖХ-МС/МС метода.
6.5 Построение градуировочной характеристики
6.5.1 Градуировочную кривую строят при помощи матричной градуировки. Для этого проводят обработку "чистых" проб, приготовленных и проанализированных ранее в соответствии с требованиями раздела 7, не содержащих тетрациклинов более 1 мкг/кг для каждого из антибиотиков, в зависимости от типа исследуемой матрицы. На стадии перерастворения перед введением в хроматограф в мерную пробирку вместимостью 5 см, содержащую исследуемую "чистую" пробу, добавляют градуировочный раствор тетрациклинов по 6.3.5.1 с таким расчетом, чтобы окончательные массовые концентрации находились в пределах от 1 до 1000 нг/см. Затем добавляют 50 мм раствора внутреннего стандарта по 6.3.5.2 и необходимое количество мобильной фазы А по 6.3.4.1, доводя объем до 1 см.
6.5.2 Для получения градуировочных данных используют не менее четырех уровней концентраций матричных градуировочных растворов.
6.5.3 При построении градуировочной зависимости для количественного определения тетрациклинов анализируют матричные градуировочные растворы различных уровней концентраций в условиях, описанных в 6.2 и 6.4. Затем строят графики зависимости массовой концентрации антибиотика тетрациклиновой группы от отношения площади хроматографического пика антибиотика тетрациклиновой группы к площади пика внутреннего стандарта для каждого фрагментного иона четырех антибиотиков тетрациклиновой группы. Образец графика приведен в приложении Б.
Построение графиков может проводиться при помощи программы обработки данных ВЭЖХ-МС/МС или при помощи программы Excel (Microsoft Office).
6.5.4 Расчетные концентрации для обоих фрагментных ионов каждого антибиотика тетрациклиновой группы должны совпадать в пределах 20%.
Градуировочная зависимость считается приемлемой, если рассчитанное значение квадрата коэффициента корреляции для градуировочной кривой каждого фрагментного иона каждого антибиотика тетрациклиновой группы не менее 0,98.
6.6 Подготовка лабораторной посуды и реактивов
6.6.1 Мойку и сушку посуды следует проводить в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Не допускается проведение подготовки посуды в данном помещении для других видов анализов. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.6.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.6.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105°С до 110°С.
7 Порядок выполнения измерений
7.1 Обработка проб органов, тканей животных, яиц, яичного порошка, молока, молочных продуктов и меда
, рыбы, нерыбных объектов и продукции из них*
________________
* Измененная редакция, Изм. N 1 .
7.1.1 Мышечную ткань предварительно очищают от грубой соединительной ткани, кожи, костей и грубого хитинового покрова. Яйца отделяют от скорлупы. Каждую пробу измельчают на гомогенизаторе и взвешивают по 1,0 г гомогенизированной пробы в виале на лабораторных весах с наибольшим пределом взвешивания 200 г. В виалу добавляют 50 мм раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 10 см экстрационного буферного раствора по 6.3.3, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 15 мин. Далее виалы с образцами помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин. Процедуру экстракции и центрифугирования повторяют еще один раз. Объединенные экстракты собирают в чистые виалы.
(Измененная редакция, Изм. N 1).
7.1.2 1,0 г меда взвешивают на лабораторных весах с наибольшим пределом взвешивания 200 г в виале вместимостью 50 см. В виалу добавляют 50 мм раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 20 см экстрационного буферного раствора по 6.3.3, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 1 мин. Далее виалы с образцами помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин.
7.2 Проведение твердофазной экстракции и подготовка к хроматографированию
7.2.1 Для проведения твердофазной экстракции картридж для ТФЭ заполняют 0,5 г сорбента. Предварительно картридж кондиционируют 6 см метилового спирта и уравновешивают 6 см бидистиллированной воды. Затем наносят объединенный экстракт и вновь промывают 6 см бидистиллированной воды. Тетрациклины элюируют с сорбента при помощи 6 см мобильной фазы Б. Полученный элюат упаривают на нагревательном модуле в токе воздуха до 0,5 см при температуре 40°С.
7.2.2 Для перерастворения и подготовки к хроматографированию объем полученного упаренного элюата в мерной пробирке вместимостью 10 см доводят до 1 см при помощи мобильной фазы А и помещают на ультразвуковую баню на 1 мин. Полученный экстракт фильтруют через мембранный фильтр и используют для ВЭЖХ-МС/МС анализа.
7.3 Обработка проб молока
7.3.1 Для очистки образцов к навеске образца молока массой 1 г, помещенной в виалу, добавляют 100 мм раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 3 см ацетонитрила, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 3 мин, затем оставляют на 15 мин в горизонтальном положении для последующего уравновешивания. Далее виалу с образцом помещают на предварительно охлажденную до 4°С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин. Полученный раствор переносят в мерную пробирку вместимостью 10 см и упаривают до 1 см на нагревательном модуле в токе воздуха при температуре 40°С. К полученному остатку добавляют 9 см буферного раствора 6.3.3 и помещают на ультразвуковую баню. Сухие молочные продукты восстанавливают по ГОСТ 29245 (пункт 3.4).
(Поправка . ИУС N 10-2018).
7.3.2 Процедуру твердофазной экстракции осуществляют в соответствии с 7.2.1, а перерастворение и подготовку к хроматографированию - в соответствии с 7.2.2.
7.4 ВЭЖХ-МС/МС анализ
7.4.1 Для определения остаточного содержания тетрациклинов и их эпи-форм проводят анализ в условиях, указанных в 6.4.
7.4.2 Время удерживания антибиотиков тетрациклиновой группы определяют при анализе градуировочных растворов.
7.5 Контроль качества измерений
7.5.1 Каждая серия измерений включает в себя несколько степеней подтверждения качества измерений.
7.5.2 Для исключения контаминации образца используемыми реагентами проводят обработку "чистого образца" в соответствии с 7.1-7.3 в зависимости от типа исследуемой матрицы.
7.5.3 Для учета матричного эффекта при расчете остаточных содержаний антибиотиков тетрациклиновой группы используют матричную градуировку по 6.5.
7.5.4 Проводят испытание образца с обработкой пробы в соответствии 7.1-7.3 в зависимости от типа исследуемой матрицы.
7.6 Обработка результатов хроматографического анализа
7.6.1 Расчеты содержания антибиотика тетрациклиновой группы выполняют с помощью градуировочной характеристики следующим образом. Вычисляют отношение площади пика фрагментного иона к площади внутреннего стандарта с помощью программы обработки спектров поставляемой вместе с хромато-масс-спектрометром. Затем, для найденного значения (абсциссы) находят точку на градуировочной характеристике. Ордината этой точки является искомым содержанием (приложение Б).
7.6.2 Окончательные результаты измерений содержания тетрациклинов округляют до целого значения и выражают в микрограммах на килограмм.
8 Метрологические характеристики
8.1 Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания тетрациклинов с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата 2, указанной в таблице 2.
Примечание - Значения относительной расширенной неопределенности, указанные в таблице 2, соответствуют границам относительной погрешности результатов измерений при 0,95.
Таблица 2 - Значения относительной расширенной неопределенности измерений (при коэффициенте охвата 2) , %, в диапазонах измерений содержаний антибиотиков тетрациклиновой группы, мкг/кг
Антибиотик тетрациклиновой группы | Относительная расширенная неопределенность , %, при 0,95 и диапазоне измерений содержания тетрациклинов, мкг/кг |
||
от 1,0 до 10,0 включ. | св. 10,0 до 100,0 включ. | св. 100,0 до 1000,0 включ. |
|
Тетрациклин | |||
Окситетрациклин | |||
Доксициклин | |||
Хлортетрациклин | |||
9 Оформление результатов измерений
9.1 Результат анализа в документах, предусматривающих его использование, представляют в виде формулы
- расширенная неопределенность при коэффициенте охвата 2 определения содержания -го антибиотика тетрациклиновой группы, определяемая по формуле (2), мкг/кг.
9.2 Значения расширенной неопределенности измерения рассчитывают с использованием значений относительной расширенной неопределенности при 2 (в соответствии с таблицей 2) по формуле
где - среднеарифметическое значение двух параллельных измерений содержания -го антибиотика в анализируемой пробе, мкг/кг;
- значение относительной расширенной неопределенности содержания -го антибиотика тетрациклиновой группы для соответствующего диапазона измерений (таблица 2).
10 Контроль качества результатов измерений
10.1 Контроль полноты извлечения внутреннего стандарта тетрациклинов
10.1.1 Контроль извлечения внутреннего стандарта тетрациклинов выполняют в ходе каждого измерения (получения результата количественного химического анализа при соблюдении требований настоящего стандарта).
10.1.2 Рассчитанные программным обеспечением значения извлечения внутренних стандартов должны находиться в диапазоне от 40% до 130%. Если рассчитанное значение извлечения ниже или выше указанного диапазона, то результаты измерения массовой доли тетрациклинов не принимают за окончательный результат. Проводят повторные исследования анализируемых проб.
10.2 Контроль неопределенности результатов измерений
При проведении испытаний рекомендуется в ходе анализа каждой серии образцов с использованием стандартной процедуры пробоподготовки (см. 7.1 и 7.3) проводить анализ градуировочных растворов в соответствии с 6.4. Результаты измерений признают удовлетворительными при выполнении следующего неравенства:
где - рассчитанное с помощью градуировочной характеристики значение содержания -го антибиотика тетрациклиновой группы в анализируемой пробе, мкг/кг;
- значение содержания -го антибиотика по паспорту на стандартный образец, мкг/кг;
- значение относительной расширенной неопределенности содержания -го антибиотика тетрациклиновой группы для соответствующего диапазона измерений (таблица 2), %.
Приложение А (справочное). Структурные формулы антибиотиков тетрациклинового ряда
Приложение А
(справочное)
Приложение Б (справочное). Отношение площади пика иона антибиотика к площади пика иона внутреннего стандарта
Приложение Б
(справочное)
Рисунок Б.1 - Отношение площади пика иона антибиотика к площади пика иона внутреннего стандарта
Приложение В (обязательное). Контроль стабильности результатов измерений
Приложение В
(обязательное)
Периодичность контроля стабильности результатов измерений регламентируют в руководстве по качеству лаборатории*.
________________
* Документ не приводится. За дополнительной информацией обратитесь по ссылке . - Примечание изготовителя базы данных.
Контроль стабильности результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ ИСО 5725-6, используя контроль стабильности среднеквадратического (стандартного) отклонения промежуточной прецизионности рутинного анализа с изменяющимися факторами "время" и "оператор".
Применяя метод контрольных карт Шухарта, проверяют стабильность этих результатов измерений и оценивают стандартное отклонение промежуточной прецизионности с изменяющимися факторами "время" и "оператор". После отбора испытуемую пробу от каждой партии подготавливают в лаборатории для анализа. Одну пробу, подвергавшуюся анализу во время смены (), анализирует повторно другой оператор в другую смену (), и результаты сравнивают. Значение стандартного отклонения промежуточной прецизионности () устанавливают в лаборатории по результатам измерений за предыдущий период. Параметры контрольной карты пределов для каждого диапазона рассчитывают следующим образом:
- среднюю линию по формуле
где - среднеквадратическое отклонение промежуточной прецизионности, %;
- верхний предел действия по формуле
Верхний предел предупреждения по формуле
Расхождение () рассчитывают по формуле
Расхождение наносят на карту в течение контролируемого периода.
Рекомендуется устанавливать контролируемый период так, чтобы количество результатов контрольных измерений было от 20 до 30. После этого проводят оценку стандартного отклонения промежуточной прецизионности () результатов по формуле
где - число измерений.
Полученное значение используют для последующего контроля стабильности результатов измерений.
Библиография
Пипетки переменного объема одноканальные, Transferpettor Brand, Германия |
|
Виалы (флаконы полипропиленовые) вместимостью 15 и 50 см, Corning 430790 и 430290 |
|
Фильтры мембранные с размером пор 0,5 мкм, Acrodisc CR 13 мм, 0,2 мкм, Life Sciences PN 4423T |
|
Измельчитель-гомогенизатор лабораторный МMR 0801/01, Bosch, Германия |
|
Вибрационный встряхиватель для пробирок (вортекс) Multi Reax, Heidolph, Германия |
|
Центрифуга лабораторная роторная рефрижераторная, Beckman, Германия |
|
Термостатируемый нагревательный модуль с системой отдувки растворителей инертным газом, Reacti-Therm (Pierce, США) |
|
Ультразвуковая баня, Elma S 30 Н, Германия |
|
Стандартный образец тетрациклина гидрохлорида, USP, Sigma, T4062 |
|
Стандартный образец окситетрациклина гидрохлорида, USP, Sigma, O5875 |
|
Стандартный образец хлортетрациклина гидрохлорида, USP, Sigma, C4881 |
|
Стандартный образец доксициклина, USP, Sigma, D9891 |
|
Стандартный образец демеклоциклина, USP, Sigma, D6140 |
|
ИСО 17604:2003 | Микробиология пищевых продуктов и кормов для животных. Отбор проб с туши для микробиологического анализа (Microbiology of food and animal feeding stuffs. Carcass sampling for microbiological analysis) |
УДК 637,638:614.3:006.354 | ||
Ключевые слова: пищевые продукты, продовольственное сырье, антибиотики тетрациклиновой группы, метод определения содержания с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием |
||
Электронный текст документа
подготовлен АО "Кодекс" и сверен по:
официальное издание
М.: Стандартинформ, 2013
Редакция документа с учетом
изменений и дополнений подготовлена
АО "Кодекс"
ГОСТ 31694-2012. Продукты пищевые, продовольственное сырье. Метод определения остаточного содержания антибиотиков тетрациклиновой группы с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
| Название документа: |
ГОСТ 33490-2015
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МОЛОКО И МОЛОЧНАЯ ПРОДУКЦИЯ
Обнаружение растительных масел и жиров на растительной основе методом газожидкостной хроматографии с масс-спектрометрическим детектированием
Milk and milk products. Detection of vegetable fat by gas chromatography with mass spectrometric detection
МКС 67.100.10
Дата введения 2016-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Государственным бюджетным учреждением Ярославской области "Ярославский государственный институт качества сырья и пищевых продуктов" (ГБУ ЯО "ЯГИКСПП")
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 12 ноября 2015 г. N 82-П)
За принятие проголосовали:
Краткое наименование страны по МК (ИСО 3166) 004-97 | Сокращенное наименование национального органа по стандартизации |
|
Минэкономики Республики Армения |
||
Киргизия | Кыргызстандарт |
|
Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 01 декабря 2015 г. N 2092-ст межгосударственный стандарт ГОСТ 33490-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2016 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
1 Область применения
1 Область применения
Настоящий стандарт распространяется на молоко и молочную продукцию и устанавливает качественный метод обнаружения в их составе растительных масел и жиров на растительной основе методом газожидкостной хроматографии с масс-спектрометрическим детектированием.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.010-76 Система стандартов безопасности труда. Взрывобезопасность. Общие требования
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
_______________
ГОСТ Р 12.1.019-2009 "Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты".
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 12.4.021-75 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания.
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4165-78 Реактивы. Медь сернокислая 5-водная. Технические условия
ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ ИСО 5725-6-2003* Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
_______________
В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 "Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике".
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13928-84 Молоко и сливки заготовляемые. Правила приемки, методы отбора проб и подготовка их к анализу
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 20010-93 Перчатки резиновые технические. Технические условия
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809.1-2014 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 1. Молоко, молочные, молочные составные и молокосодержащие продукты
ГОСТ 26809.2-2014 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 2. Масло из коровьего молока, спреды, сыры и сырные продукты, плавленые сыры и плавленые сырные продукты
ГОСТ 27752-88 Часы электронно-механические кварцевые настольные, настенные и часы-будильники. Общие технические условия
ГОСТ 28165-89 Приборы и аппараты лабораторные из стекла. Аквадистилляторы. Испарители. Установки ректификационные. Общие технические требования
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29169-91 Посуда лабораторная стеклянная. Пипетки с одной отметкой
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины и определения в соответствии с , а также термины:
3.1 газожидкостная хроматография:
Метод разделения и анализа смеси веществ, основанный на их различных температурах кипения и взаимодействии с неподвижной жидкой фазой в потоке газа-носителя
3.2 масс-спектрометрия:
Метод, основанный на разделении ионизированных атомов, молекул и радикалов в газовой фазе, характеризующихся разным отношением массы частицы к ее заряду (m/z), и регистрации спектра образовавшихся ионов.
4 Сущность метода
Метод основан на предварительном гидролизе стероидов, содержащихся в жировой фазе молока и молочных продуктов, в стерины, хроматографическом их разделении газовой хроматографией и сравнении полученных масс-спектров стеринов со спектрами и временем удерживания стандартных веществ.
5 Отбор проб
Отбор и подготовка проб к анализу - по ГОСТ 13928 , ГОСТ 26809.1 , ГОСТ 26809.2 .
Перед анализами отобранные пробы молока и молочных продуктов, за исключением молочных консервов и молочных продуктов в запаянных или закатанных банках, хранят при температуре (4±2)°С, пробы мороженого - при температуре не выше 2°С.
6 Условия проведения анализа
При выполнении анализа в лаборатории следует соблюдать следующие условия:
температура окружающего воздуха | |
относительная влажность воздуха | |
атмосферное давление | (95±10) кПа. |
7 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Хроматограф газовый, оснащенный масс-спектрометрическим детектором, позволяющим проводить измерения в диапазоне масс от 15 до 500 а.е.м. в режиме ионизации электронным ударом при энергии электронов 70 эВ, масс-спектральном разрешении не менее 1 а.е.м. по всей шкале масс, и программным обеспечением для сбора и обработки данных.
Колонка капиллярная с неполярной неподвижной фазой и верхней температурной границей рабочего диапазона не менее 320°С. Длина и диаметр газохроматографической колонки, толщина слоя неподвижной фазы должны обеспечивать приемлемое хроматографическое разрешение и число теоретических тарелок для полного разделения стеринов.
Термометр ртутный стеклянный лабораторный типа Б по ГОСТ 28498 , с диапазоном измерения температуры от 0°С до 100°С, с ценой деления шкалы 1°С.
Весы по ГОСТ OIML R 76-1 , обеспечивающие точность взвешивания с пределом допускаемой абсолютной погрешности ±0,0005 г.
Микрошприц вместимостью 10 мм с погрешностью дозирования не более 5%.
Шкаф сушильный лабораторный любого типа по ГОСТ 14919 , поддерживающий температуру до 200°С с погрешностью ±5°С.
Печь муфельная, обеспечивающая нагрев в диапазоне температур от 300°С до 800°С.
Баня водяная с регулируемым обогревом с погрешностью поддержания температуры ±2°С.
Центрифуга лабораторная с ротором для центрифужных пробирок вместимостью 15 и 50 см, обеспечивающая фактор центрифугирования не менее 5000 g
.
Электроплитка бытовая по ГОСТ 14919 с закрытой спиралью и регулятором нагревания.
Устройство перемешивающее лабораторное.
Испаритель роторный по ГОСТ 28165 .
Воронки делительные ВД-3-250ХС по ГОСТ 25336 с фторопластовым краном.
Колба коническая Кн-1-100-29/32 ТС, Кн-1-250-29/32 ТС по ГОСТ 25336 .
Колбы круглодонные К-1-50-29/32, К-1-100-29/32, К-1-250-29/32 по ГОСТ 25336 .
Колбы мерные с притертыми пробками 2-5-2, 2-100-2, 2-1000-2 по ГОСТ 1770 .
Цилиндры 2-25, 2-50 по ГОСТ 1770 .
Стаканы В-1-50, В-1-100, В-1-1000 по ГОСТ 25336 .
Воронки В-56-80, В-75-110 по ГОСТ 25336 .
Пипетки 1-2-2-1, 1-2-2-10 по ГОСТ 29227 .
Холодильник ХШ-1-300-19/26ХС по ГОСТ 25336 .
Ступка 5 по ГОСТ 9147 .
Пестик 1 по ГОСТ 9147 .
Эксикатор 2-190 по ГОСТ 25336 .
Груша резиновая медицинская.
Палочки стеклянные оплавленные по ГОСТ 21400 .
Щипцы металлические тигельные.
Терка мелкая металлическая.
Пробирки центрифужные вместимостью 15 и 50 см.
Емкости стеклянные (виалы) для жидких проб вместимостью 2 см, снабженные крышками с силиконовой и тефлоновой мембраной.
Бумага фильтровальная лабораторная по ГОСТ 12026 .
Бумага индикаторная универсальная для определения рН.
Натрия сульфат по ГОСТ 4166 , безводный.
Натрия гидроокись по ГОСТ 4328 , х.ч.
Спирт этиловый ректификованный по ГОСТ 5962 .
Медь (II) сернокислая 5-водная по ГОСТ 4165 , х.ч.
Вода дистиллированная по ГОСТ 6709 .
Кислота серная по ГОСТ 4204 , х.ч.
Калий двухромовокислый по ГОСТ 4220 , х.ч.
Калия гидроокись по ГОСТ 24363 , ч.д.а.
Метанол с массовой долей основного вещества не менее 99,8%.
Тетрагидрофуран с массовой долей основного вещества не менее 99,5%.
Гелий газообразный марки А (объемная доля гелия не менее 99,995%).
Холестерин с массовой долей основного вещества не менее 99,0% (CAS N 80-99-9).
Смесь фитостеринов - брассикастерин (CAS N 474-67-9), кампестерин (CAS N 474-62-4), стигмастерин (CAS N 83-48-7), -ситостерин (CAS N 83-46-5) - в хлороформе суммарной массовой концентрации 25 мг/ см.
Допускается применение других средств измерения и вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
8 Подготовка к проведению анализа
8.1 Подготовка посуды
Стеклянную химическую посуду, используемую в процессе анализа, ополаскивают водопроводной водой, заливают хромовой смесью до 1/4-1/3 вместимости сосуда и осторожно смачивают внутренние его стенки. После этого хромовую смесь выливают обратно в емкость для хранения. Посуду оставляют на несколько минут, затем тщательно отмывают сначала водопроводной, а затем дистиллированной водой и сушат в сушильном шкафу при температуре 105°С.
8.2 Подготовка реактивов и материалов, приготовление растворов
8.2.1 Натрий сернокислый безводный прокаливают в муфельной печи 4 ч при температуре 400°С и охлаждают в эксикаторе.
Срок хранения натрия сернокислого безводного в эксикаторе при комнатной температуре - не более 3 мес.
8.2.2 Осадительный реактив
В химическом стакане вместимостью 500 см взвешивают (70,0±0,1) г сернокислой меди и растворяют в небольшом объеме дистиллированной воды, количественно переносят в мерную колбу вместимостью 1000 см и доводят объем раствора дистиллированной водой до метки.
Срок хранения осадительного реактива в склянке из темного стекла при комнатной температуре - не более 3 мес.
8.2.3 Раствор гидроксида калия в метаноле молярной концентрации 2 моль/дм
В мерной колбе вместимостью 100 см взвешивают (11,21±0,01) г предварительно измельченного гидроксида калия и доводят объем раствора до метки метанолом, интенсивно перемешивают до полного растворения гидроксида калия и дают остыть до комнатной температуры.
Срок хранения раствора в плотно закрытой склянке при температуре (4±2)°С - не более 3 мес.
8.2.4 Стандартный раствор холестерина массовой концентрации 5 мг/см
В химическом стакане вместимостью 100 см взвешивают (0,50±0,01) г холестерина, вносят около 50 смн
-гексана, аккуратно перемешивают, количественно переносят в мерную колбу вместимостью 100 см и доводят объем раствора н
-гексаном до метки.
8.2.5 Раствор смеси фитостеринов суммарной концентрации 5 мг/см
В мерную колбу вместимостью 5 см вносят 1 см раствора смеси фитостеринов, доводят объем раствора до метки н
-гексаном и перемешивают.
Срок хранения раствора в плотно закрытой склянке при температуре (4±2)°С - не более 6 мес.
8.2.6 Рабочий раствор смеси холестерина и фитостеринов массовой концентрации холестерина 2,5 мг/ см
и фитостеринов (суммарно) 2,5 мг/см
В стеклянную виалу вместимостью 2 см вносят 0,5 см раствора смеси фитостеринов, приготовленного по 8.2.5, и 0,5 см раствора холестерина, приготовленного по 8.2.4, и тщательно перемешивают.
Раствор готовят непосредственно перед проведением анализа.
8.3 Подготовка хромато-масс-спектрометра
Хромато-масс-спектрометр для анализа в режиме ионизации пробы электронным ударом готовят в соответствии с инструкцией по эксплуатации и устанавливают режим для анализа.
Примерный вид режима приведен ниже:
а) режим хроматографирования:
инжектируемый объем анализируемой пробы - 1 мм;
деление потока - 1:1;
температура испарителя - 310°С;
время задержки включения детектора - 28 мин;
тип колонки - HP-5MS;
газ-носитель - гелий;
скорость потока гелия через колонку - 1 см/мин;
программирование температуры термостата:
- начальная температура колонки - 115°С, время анализа при этой температуре - 1 мин;
- скорость нагрева колонки от 9°С/мин до 260°С, от 3°С/мин до 290°С;
б) режим масс-спектрометра:
энергия ионизации - 70 эВ;
температура ионного источника - 230°С;
температура квадруполя - 150°С;
температура ГХ/МС интерфейса - 290°С;
диапазон сканирования масс ионов: 35-450 а.е.м.
При соблюдении вышеуказанных условий продолжительность анализа составляет 45 мин.
8.4 Градуировка хроматографа
Градуировка хроматографа заключается в определении времени удерживания анализируемых стеринов (приложение А) и выполняется путем анализа рабочего раствора смеси холестерина и фитостеринов по 8.2.6 в условиях, приведенных в 8.3. Масс-спектрометрический анализ проводят в режиме селективного ионного мониторинга (SIM) характеристических ионов стеринов. Значения масс характеристических ионов приведены в таблице 1.
Таблица 1 - Значения масс характеристических ионов холестерина и фитостеринов
Наименование | Характеристические ионы, а.е.м. |
|
подтверждающие |
||
Холестерин | ||
Брассикастерин | ||
Кампестерин | ||
Стигмастерин | ||
Ситостерин | ||
При наличии плохо разделенных хроматографических пиков стеринов корректируют режим хроматографирования.
Критерии приемлемости результатов анализа и проверки работоспособности хроматографической системы заключаются в следующем:
Хроматографическая система считается работоспособной, если выполняются следующеие условия:
- разрешение между пиками стеринов на хроматограмме рабочего раствора не менее 1,5;
- асимметрия пиков на хроматограмме рабочего раствора не более 1,5;
- число теоретических тарелок по пику холестерина не менее 500000;
- СКО по площади пика холестерина по шести параллельным измерениям рабочего раствора не более 5%, а по времени удерживания - не более 1%.
Результат анализа рабочего раствора является приемлемым при условии, что соотношение сигнал/шум для пика холестерина не менее 150.
Пики фитостеринов с интенсивностью сигнала менее 2% от высоты пика холестерина или с соотношением сигнал/шум менее 3 во внимание не принимают.
8.5 Подготовка проб
8.5.1 Метод с предварительным выделением жира
8.5.1.1 Жир молочный, масло сливочное и топленое, пасты масляные
Пробу продукта массой (40-50) г расплавляют в химическом стакане вместимостью 100 см в сушильном шкафу при температуре (45±2)°С для расслоения на жировую и водную фазу. Затем жировую фазу фильтруют через сухую фильтровальную бумагу так, чтобы водная фаза не попадала на фильтр. Если отфильтрованный жир будет прозрачным, то продолжают подготовку пробы по 8.5.1.9. При наличии в отфильтрованном жире мути его фильтруют повторно.
8.5.1.2 Сырое молоко и сырые сливки, питьевое молоко и питьевые сливки
1 вариант.
В коническую колбу вместимостью 500 см помещают 400 см пробы продукта. Пробу нагревают на водяной бане до температуры (75±2)°С, добавляют 15 см осадительного реактива по 8.2.2 и продолжают нагревать до получения сгустка, который фильтруют через фильтровальную бумагу, промывают его теплой водой. Осадок переносят в фарфоровую ступку, перемешивают его с достаточным количеством безводного сульфата натрия до получения зернистой массы.
2 вариант.
Пробу продукта помещают в химический стакан вместимостью 1000 см и оставляют до скисания. Затем снимают верхний жировой слой, помещают в фарфоровую ступку и тщательно перемешивают с безводным сернокислым натрием, взятым в количестве, достаточном для образования зернистой массы.
8.5.1.3 Концентрированное молоко, сгущенное молоко и мороженое
В конической колбе вместимостью 250 см взвешивают (100,0±1,0) г продукта.
Мороженое предварительно освобождают от глазури и других отделяемых компонентов. В пробу продукта добавляют 100 см дистиллированной воды, нагревают смесь на водяной бане до температуры (75±2)°С, добавляют 15 см осадительного реактива и продолжают нагревать до получения сгустка, который фильтруют через фильтровальную бумагу, промывают его теплой водой до обесцвечивания фильтрата. Осадок переносят в фарфоровую ступку, перемешивают его с безводным сернокислым натрием, взятым в количестве, достаточном для образования зернистой массы.
8.5.1.4 Сметана и продукты на ее основе
100 г пробы продукта тщательно перемешивают в фарфоровой ступке с безводным сульфатом натрия, взятым в количестве, достаточном для образования зернистой массы.
8.5.1.5 Сухие молочные продукты
В фарфоровой ступке взвешивают (300,0±1,0) г пробы продукта и добавляют 300 см дистиллированной воды. Смесь тщательно перемешивают стеклянной палочкой до однородной консистенции и оставляют на 60 мин до набухания белков и перемешивают в фарфоровой ступке с безводным сульфатом натрия, взятым в количестве, достаточном для образования зернистой массы.
8.5.1.6 Творог и творожные продукты
100 г пробы продукта перемешивают в фарфоровой ступке с безводным сульфатом натрия, взятым в количестве, достаточном для образования зернистой консистенции.
8.5.1.7 Сыр
100 г пробы продукта измельчают при помощи терки, помещают в фарфоровую ступку и растирают с безводным сульфатом натрия, взятым в количестве, достаточном для образования зернистой консистенции.
8.5.1.8 Выделение жира
Пробу продукта, полученную по 8.5.1.2-8.5.1.7, переносят в колбу на 250 см и добавляют 100-150 смн
-гексана, встряхивая на перемешивающем устройстве или вручную и экстрагируют жир. Растворитель полностью удаляют на роторном испарителе при температуре 40°С.
В случае если дальнейший анализ пробы не может быть проведен сразу, то жир, выделенный по 8.5.1.8, хранят в холодильнике при температуре (4±2)°С не более 3 мес.
8.5.1.9 Получение свободных стеринов
(1,0±0,1) г жира, выделенного по 8.5.1.8, вносят в коническую колбу вместимостью 150 см, добавляют 0,3 г гидроокиси натрия, 30 см этилового спирта и проводят гидролиз: кипятят с обратным холодильником на электроплитке в течение 60 мин. Содержимое колбы после омыления должно представлять собой однородный прозрачный раствор, который охлаждают в вытяжном шкафу при комнатной температуре до 40°С. В колбу добавляют 30 см дистиллированной воды. Содержимое колбы помещают в делительную воронку вместимостью 250 см, добавляют 15 смн
-гексана и экстрагируют неомыляемые вещества, осторожно встряхивая в течение одной минуты. Для лучшего разделения слоев добавляют 2-4 см этилового спирта. После расслоения фаз верхний гексановый слой сливают в коническую колбу, а нижний слой дважды подвергают повторной экстракции с новыми порциями по 15 смн
-гексана. Гексановые экстракты помещают в делительную воронку. Экстракцию неомыляемых веществ проводят по возможности быстро, предохраняя пробу от попадания на нее прямого солнечного света. Объединенный н
н
-гексановую фракцию пропускают через бумажный фильтр с безводным сульфатом натрия, переносят в колбу для упаривания, концентрируют на роторном испарителе при температуре (40±5)°С до получения раствора объемом 1,5-2,0 см и переносят в виалу. Концентрированный раствор анализируют с помощью газожидкостной хроматографии с масс-спектрометрическим детектированием.
8.5.2 Ускоренный метод выделения жира
В соответствии с таблицей 2 в коническую колбу вместимостью 150 см вносят анализируемую пробу продукта, добавляют 0,5 г гидроокиси натрия, 30 см этилового спирта и проводят гидролиз: кипятят на водяной бане с обратным холодильником на электроплитке 60 мин. Содержимое колбы охлаждают до температуры 40°С и добавляют 30 см дистиллированной воды. Содержимое колбы помещают в делительную воронку вместимостью 250 см, добавляют 15 смн
-гексана и экстрагируют неомыляемые вещества, осторожно встряхивая в течение одной минуты. Для лучшего разделения слоев добавляют 2-4 см этилового спирта.
Таблица 2 - Рекомендуемая масса анализируемой пробы продукта
В граммах
Наименование продукта | Анализируемая проба |
Молоко, кисломолочные продукты (за исключением сметаны) | |
Творог и творожные продукты | |
Мороженое | |
Масло сливочное и топленое, пасты масляные, молочный жир | |
Сухие молочные продукты | |
Примечание - Мороженое предварительно освобождают от глазури и других отделяемых компонентов. Сыр измельчают при помощи терки. |
|
После расслоения фаз верхний н
-гексановый слой сливают в коническую колбу, а с нижним слоем дважды повторяют экстракцию с новыми порциями н
-гексана по 15 см каждая. Экстракцию неомыляемых веществ проводят по возможности быстро, предохраняя пробу от попадания на нее прямого солнечного света. Объединенный н
-гексановый слой промывают в делительной воронке несколькими порциями по 20 см дистиллированной воды до нейтральной реакции промывных вод по универсальной индикаторной бумаге. Отмытую н
-гексановую фракцию пропускают через бумажный фильтр с безводным сульфатом натрия, переносят в колбу для упаривания, концентрируют раствор на роторном испарителе при температуре (40±5)°С до объема 1,5-2,0 см и переносят в виалу. Концентрированный раствор анализируют с помощью газожидкостной хроматографии с масс-спектрометрическим детектированием.
8.5.3 Метод без предварительного выделения жира
Применяют при разногласиях в оценке качества анализируемой продукции.
В центрифужную пробирку вместимостью 50 см помещают (25,0±1,0) г молока или молочного продукта, добавляют 25 см тетрагидрофурана, закрывают крышкой, интенсивно встряхивают и центрифугируют в течение 5-10 мин на центрифуге с частотой оборотов ротора, соответствующей фактору центрифугирования не менее 5000 g
.
Верхний слой в зависимости от его объема переносят в центрифужную пробирку вместимостью 15 или 50 см и добавляют дистиллированную воду в соотношении 1:2, закрывают крышкой, интенсивно встряхивают и центрифугируют в течение 5-10 мин на центрифуге с частотой оборотов ротора, соответствующей фактору центрифугирования не менее 5000 g
.
(5,00±0,01) см пробы очищенного раствора молочного жира переносят в центрифужную пробирку вместимостью 50 см для щелочного гидролиза.
В центрифужную пробирку с пробой раствора молочного жира добавляют такое же количество по объему раствора гидроксида калия в метаноле, приготовленного по 8.2.3, интенсивно перемешивают в течение минуты, добавляют 10 смн-
гексана, интенсивно перемешивают в течение одной минуты и центрифугируют в течение 10 мин на центрифуге с частотой оборотов ротора, соответствующей фактору центрифугирования не менее 5000 g
.
Верхний н-
гексановый слой декантируют в делительную воронку и промывают несколькими порциями по 10 см дистиллированной воды до нейтральной реакции промывных вод по универсальной индикаторной бумаге. Отмытую н
-гексановую фракцию пропускают через бумажный фильтр с безводным сульфатом натрия, переносят в колбу для упаривания, концентрируют раствор на роторном испарителе при температуре (40±5)°С до объема 1,5-2,0 см и переносят в виалу. Полученный концентрированный раствор анализируют с помощью газожидкостной хроматографии с масс-спектрометрическим детектированием.
9 Проведение анализа
Для оценки фона (чистоты аналитической системы) каждый раз перед началом работы инжектируют в прибор 1 мм чистого растворителя (н
-гексан) и записывают масс-хроматограмму, на которой не должно присутствовать посторонних пиков.
Отбирают 1 мм анализируемой пробы продукта, подготовленной в соответствии с 8.5, вводят в испаритель газового хроматографа и выполняют хроматографическое разделение в условиях, приведенных в 8.3. Масс-спектрометрический анализ проводят в режиме селективного ионного мониторинга (SIM) характеристических ионов стеринов в соответствии с таблицей 1 по 8.4. Записывают хроматограммы и идентифицируют индивидуальные стерины по масс-спектру и совпадению времен удерживания.
Пробу продукта анализируют не менее двух раз.
10 Обработка результатов анализа
После проведения анализа с помощью системы обработки данных фиксируют на масс-хроматограммах пики в области времен удерживания, соответствующих выходу холестерина и фитостеринов.
Фитостерины считают обнаруженными при выполнении ряда условий:
- интенсивность отклика сигнала в единицах шума для пика не менее 3 и по интенсивности сигнала холестерина не менее 2%;
- время удерживания стерина на хроматограмме отличается от времени удерживания рабочего раствора на хроматограмме не более чем на 1%;
- расхождение между соотношениями интенсивности отклика сигнала ионов в спектре соответствующего стерина в анализируемой пробе и в спектре того же стерина в рабочем растворе смеси, приготовленной по 8.2.6, не превышает 10%.
Не учитывают пики фитостеринов с интенсивностью отклика сигнала не более 2% от высоты пика холестерина или с соотношением сигнал/шум не более 3.
Наличие -ситостерина или других фитостеринов в жировой фазе анализируемой пробы продукта свидетельствует о присутствии в ней растительных масел или жиров на растительной основе (см. приложение Б).
11 Оформление результатов анализа
Результат обнаружения растительных масел и жиров на растительной основе представляют в документах в виде наличия или отсутствия каждого стерина в отдельности, на основании чего делают заключение о фальсификации или нефальсификации жировой фазы пробы продукта растительными маслами или жирами на растительной основе.
12 Контроль качества анализа
Контроль качества результатов анализа обеспечивают путем проверки работоспособности хроматографической системы, оценки ее чистоты, выполнения критериев приемлемости результатов анализа и условий в соответствии с 8.4 и разделом 9.
13 Требования, обеспечивающие безопасность
13.1 Условия безопасного проведения работ
При выполнении работ следует соблюдать следующие требования:
- помещение, в котором проводят анализ, должно быть оборудовано приточно-вытяжной вентиляцией в соответствии с ГОСТ 12.4.021 . Работу с реактивами необходимо проводить в вытяжном шкафу. Содержание вредных веществ в воздухе рабочей зоны не должно превышать норм, установленных требованиями ГОСТ 12.1.005 ;
- при работе с концентрированными кислотами и щелочами необходимо использовать спецодежду, защитные очки и резиновые перчатки. При выполнении анализов следует соблюдать требования безопасности при работе с химическими реактивами согласно ГОСТ 12.1.007 .
13.2 Требования к квалификации оператора
К выполнению работ допускаются лица, имеющие квалификацию инженер, техник или лаборант, владеющие знаниями в области газовой хроматографии и масс-спектрометрии, навыками проведения анализа и изучившие инструкцию по эксплуатации используемой аппаратуры.
Приложение А (справочное). Хроматограмма рабочего раствора смеси холестерина и фитостеринов
Приложение А
(справочное)
А.1 Хроматограмма рабочего раствора смеси холестерина и фитостеринов приведена на рисунке А.1.
Рисунок А.1 - Хроматограмма, полученная при разделении рабочего раствора смеси холестерина и фитостеринов по 8.2.5, на колонке HP-5MS (с нанесенной неполярной жидкой фазой - 5% фенил и 95% диметилсилоксан, длиной 30 м, внутренним диаметром 0,25 мм, толщиной нанесения жидкой фазы 0,25 мкм) в условиях, приведенных в 8.3
Приложение Б (справочное). Хроматограммы стериновой фракции жировой фазы пробы продукта, не фальсифицированного и фальсифицированного растительными маслами или жирами на растительной основе
Приложение Б
(справочное)
Б.1 Хроматограмма стериновой фракции жировой фазы пробы продукта, не фальсифицированного растительными маслами или жирами на растительной основе, приведена на рисунке Б.1
Рисунок Б.1 - Хроматограмма стериновой фракции жировой фазы пробы продукта, не фальсифицированного растительными маслами или жирами на растительной основе
Б.2 Хроматограмма стериновой фракции жировой фазы пробы продукта, фальсифицированного растительными маслами или жирами на растительной основе, приведена на рисунке Б.2.
Рисунок Б.2 - Хроматограмма стериновой фракции жировой фазы пробы продукта, фальсифицированного растительными маслами или жирами на растительной основе
Библиография
Технический регламент Таможенного союза ТР ТС 033/2013 "О безопасности молока и молочной продукции", принятый Решением Совета Евразийской Экономической комиссии N 67 от 9 октября 2013 г .
УДК 637.147.2:543:06:006.354 | МКС 67.100.10 |
Ключевые слова: молоко, продукты молочные, жир молочный, обнаружение растительных масел и жиров на растительной основе, газожидкостная хроматография, масс-спектрометрическое детектирование, стерины, омыление, хромато-масс-спектрометр |
|
Электронный текст документа
подготовлен АО "Кодекс" и сверен по:
официальное издание
М.: Стандартинформ, 2016
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ (МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION. METROLOGY AND CERTIFICATION (ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ, КОРМА, КОРМОВЫЕ ДОБАВКИ
Определение массовой доли диоксинов методом хромато-масс-спектрометрии высокого разрешения
Издание официальное
Стамдартимформ
ГОСТ 34449-2018
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стан* дартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные. правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия. обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 июля 2018 г. No 110-П)
4 Приказом Федерального агентства по техническому регулированию и метрологии от 31 августа 2018 г. N9 548-ст межгосударственный стандарт ГОСТ 34449-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 октября 2019 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информацией-ном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ. оформление. 2018
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен. тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
1 Область применения..................................................................1
3 Сущность метода.....................................................................2
4 Требования безопасности и условия выполнения измерений.................................2
5 Средства измерений, вспомогательное оборудование, материалы, посуда и реактивы...........3
6 Подготовка к проведению измерений....................................................6
6.1 Подготовка лабораторной посуды и материалов........................................6
6.2 Подготовка сорбентов и реактивов...................................................7
6.3 Приготовление растворов изотопно-меченых суррогатных и внутренних стандартов..........6
7 Отбор и подготовка проб...............................................................8
7.1 Отбор проб......................................................................8
7.2 Подготовка проб..................................................................8
7.3 Экстракция ПХДД/ПХДФ...........................................................9
7.4 Очистка экстракта методом колоночной хроматографии................................10
7.5 Приготовление холостой пробы....................................................11
8 Порядок определения ПХДД/ПХДФ.....................................................11
8.1 Параметры хроматографических измерений..........................................11
8.2 Градуировка хромато-масс-спектрометрической системы...............................13
8.3 Проведение измерения...........................................................14
9 Обработка результатов...............................................................15
10 Метрологические характеристики.....................................................15
11 Оформление результатов измерений..................................................15
12 Контроль качества результатов измерений..............................................16
Приложение А (обязательное) Диоксиновый эквивалент токсичности (ТЭК ВОЗ)
конгенеров ПХДД/ПХДФ...................................................18
ГОСТ 34449-2018
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ. ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ. КОРМА. КОРМОВЫЕ ДОБАВКИ
Определение массовой доли диоксинов методом хромато*масс*спектрометрии высокого разрешения
Food products, food raw materials, feeds, feed additives.
Determination of dioxins mass fraction by gas chromatography/high-resolution mass spectrometry
Дата введения - 2019-10-01
1 Область применения
Настоящий стандарт распространяется на пищевые продукты и продовольственное сырье - мясо животных всех видов, в том числе мясо птицы, а также субпродукты, масло из коровьего молока, животный жир. корма, кормовые добавки и устанавливает метод хромато-масс-спектрометрии высокого разрешения для идентификации и определения массовой доли 17 высокотоксичных попихлорирован-ных дибензодиоксинов (ПХДД) и дибенэофуранов (ПХДФ) в диапазоне измерений каждого конгенера* от 1.0 до 30.0 нг/кг (от 1.0 до 30.0 трлн" 1).
Примечания
1 ПХДД: 2,3,7,8-тетрахпордибензо-п-диоксин (2,3.7.8-ТХДЦ), 1.2.3,7. 8-пентахлордибенэо-п-диоксин (1.2.3.7,8-ПеХДЦ). 1.2.3.4,7.8-гвксахлордибенэо-п-диоксин{1.2.3,4,7.8-ГкХДД). 1.2,3.6.7.8-гексахлордибвнэо-л-диоксин (1,2.3,6.7,8-ГкХДЦ). 1.2,3.7.8.9-гексахлордибенэо-п-диоксин (1,2.3.7.8.9-ГкХДД). 1.2.3.4,в.7.в-гептахлорди6енэо-п-диоксин (1,2.3,4,6.7.8-ГпХДД), окгахлордибензо-п-диоксин (ОХДД) конгенеры.
2 ПХДФ: 2.3,7,8-тетрахлордибвнзофуран (2.3.7.8-ТХДФ), 1.2,3.7.8-пентахлордибвнзофуран (1.2,3.7.8-ПеХДФ),
2.3.4.7.8- пентахлордибвнэофурам (2.3,4.7.8-ПеХДФ). 1.2,3.4,7.8-гексахлор-дибвнэофуран (1,2,3,4.7,8-ГкХДФ),
1.2.3.6.7.8- гексахлордибенэофуран (1,2.3,6.7.8-ГкХДФ). 2.3.4,6.7,8-гексахлордибенэофуран (2,3.4,6,7.8-ГкХДФ).
1.2.3.7.8.9- гексахлордибенэофуран (1,2.3,7,8.9-ГкХДФ). 1.2,3,4.6,7,в-гептахлоодибензофуран (1.2.3.4,6,7.8-ГпХДФ).
1.2.3.4.7.8.9- гелгахлордибенэофуран (1,2,3.4,7,8.9-ГпХДФ), октахлордибвнэофурэн (ОХДФ) конгенеры.
2 Нормативные ссылки
8 настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-2017 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты**
* Конгенер (лат. congener: однотипный, принадлежащий к той же группе) - индивидуальное химическое соединение, входящее в группу похожих между собой соединений, имеющих сходное происхождение и структуру.
** В Российской Федерации действует ГОСТ Р 12.1.019-2009.
Издание официальное
ГОСТ 12.2.085-2017 Арматура трубопроводная. Клапаны предохранительные. Выбор и расчет пропускной способности
ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы не 1 автоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 745-2014 Фольга алюминиевая для упаковки. Технические условия
ГОСТ 1770-74 (ИСО 1042-83. ИСО 4788-ВО) Посуда мерная лабораторная стеклянная. Цилин 1 дры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 8265-91 Жиры животные топленые. Правила приемки и методы испытания
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 9293-74 {ИСО 2435-73) Азот газообразный и жидкий. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13496.0-2016 Комбикорма, комбикормовое сырье. Методы отбора проб
ГОСТ 17681-82 Мука животного происхождения. Методы испытаний
ГОСТ 19908-90 Тигли, чаши, стаканы, колбы, воронки, пробирки и наконечники из прозрачного кварцевого стекла. Общие технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809.2-2014 Молоко и молочная продукция. Правила приемки, методы отбора и подготовка проб к анализу. Часть 2. Масло из коровьего молока, спреды, сыры и сырные продукты, плавленые сыры и плавленые сырные продукты
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубгыкован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана осыпка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Метод основан на экстракции аналитое органическими растворителями, последовательной очистке экстракта с применением колоночной хроматографии на различных сорбентах и количественном анализе методом хромато-масс-спекгрометрии высокого разрешения с использованием суррогатных изотопно-меченых стандартов 1 - аналогов определяемых соединений, вводимых в пробу на стадии подготовки проб.
Идентификацию аналитое в анализируемой пробе проводят по временам удерживания конгенеров и соотношениям площадей пиков на масс-хроматограммах их характеристических ионов. Количественное определение проводят методом внутреннего стандарта.
4 Требования безопасности и условия выполнения измерений
4.1 Конгенеры ПХДД и ПХДФ относятся к высокоопасным соединениям. Требования безопасности при работе с препаратами, содержащими ПХДД/ПХДФ. устанавливают в соответствии с нормативными документами, действующими на территории государства, принявшего стандарт.
4.2 Применяемые е работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007, при работе с ними следует соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.3 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.4 Приготовление и дозирование растворов суррогатных изотопно-меченых и внутренних стандартов диоксинов, добавление их к анализируемой пробе, подготовку пробы к анализу проводят под тягой в вытяжном шкафу.
4.5 Пробы, подготовленные к анализу, растворы исходных стандартных образцов, аттестованных смесей следует хранить в виалах вместимостью 1.5 см 3 , закрытых навинчиваемыми или запрессованными крышками с комбинированными прокладками (силикон/тефлон), прокалываемыми микрошприцем.
4.6 При выполнении измерений с использованием хромато-масс-спектрометра следует соблюдать правила по электробезопасности по ГОСТ 12.1.019 и правила безопасной эксплуатации сосудов, работающих под давлением по ГОСТ 12.2.085.
4.7 К выполнению измерений допускают специалистов, имеющих высшее специальное образование. прошедших соответствующий инструктаж, владеющих техникой хромато-масс-спектрометрии и изучивших инструкции по эксплуатации используемых приборов.
4.8 При выполнении измерений соблюдают следующие условия:
Температура окружающего воздуха............................................................................от 15 до 25 2 С;
Относительная влажность воздуха...............................................................................от 20 до 80 %.
5 Средства измерений, вспомогательное оборудование, материалы, посуда и реактивы
5.1 Для определения содержания ПХДД/ПХДФ применяют следующие средства измерений, вспомогательное оборудование, материалы и посуду:
Весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1 с максимальной нагрузкой не более 200 г и пределом допускаемой погрешности ± 0.1 мг:
Пипетки одноканальные переменной вместимости 10-100 мм 3 . 40-200 мм 3 . 200-1000 мм 3 . 1-5 см 3 с допустимой относительной погрешностью дозирования по воде не более ± 2.5 %;
Хромато-масс-спектрометр. позволяющий проводить измерения в диапазоне масс от 50 до 600 атомных единиц массы (а. е. м.). разрешением по шкале масс не менее 10 000 в режиме ионизации электронным ударом, оснащенный компьютерной системой обработки данных;
Колонку кварцевую капиллярную 2 длиной 30 или 60 м. диаметром 0.25 мм с неподвижной полярной фазой толщиной 0.25 мкм:
Компьютер с установленным программным обеспечением для управления хромато-масс-спектрометром и обработки результатов измерений:
Микрошприцы хроматографические вместимостью 10 мм 3 с ценой деления 0.1 мм 3:
« испаритель ротационный со скоростью вращения от 20 до 280 об/мин и температурным диапазоном нагревательной бани от 30 до 100 "С;
Модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования не менее 220 "С;
Экстрактор автоматический для ускоренной экстракции растворителями под давлением с температурой экстракции от 20 до 200 в С;
* баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм 3 ;
Шейкер переворачивающий для колб и пробирок со скоростью вращения до 100 об/мин:
Измельчитель-гомогенизатор лабораторный;
Мельницу лабораторную для измельчения кормов;
Печь микроволновую для экспрессной подготовки проб мощностью не менее 800 8т;
Шкаф сушильный с максимальной температурой нагрева не менее 250 °C и погрешностью под* держания заданной температуры ± 5 ’С;
* печь муфельную с максимальной температурой нагрева 850 ’С и погрешностью поддержания заданной температуры ± 5 %;
* камеру лабораторную морозильную рабочим диапазоном температур от минус 15 в С до минус 25 *С;
Ячейки экстракционные вместимостью 33 и 66 см 3 ;
* виалы для хроматографа с коническим дном вместимостью 1,5 см 3 , с навинчиваемыми крышка* ми и комбинированными прокладками (силикон/тефлон);
* колонку стеклянную для колоночной хроматографии длиной не менее 100 мм и внутренним диаметром 8 мм. сужающуюся книзу;
Колонку стеклянную для колоночной хроматографии длиной не менее 150 мм и внутренним диа* метром 10 мм, сужающуюся книзу;
* колонку стеклянную для колоночной хроматографии длиной не менее 300 мм и внутренним диаметром 10 мм. сужающуюся книзу;
Фильтры диаметром 3.3 см из бумаги фильтровальной по ГОСТ 12026;
* фильтры из стекловолокна диаметром 3.3 см;
Стекловату силанизированную;
Фольгу алюминиевую по ГОСТ 745;
Колбу К-1-100-14/23 ТС по ГОСТ 25336;
Колбу Кн-1-100-14/23 ТС по ГОСТ 25336;
Колбы 1-100(500)-1 по ГОСТ 1770;
Пробирки 10 по ГОСТ 19908;
Цилиндры 1-10(100}- 1 поГОСТ 1770;
Эксикаторы 2-250 ло ГОСТ 25336;
Аппарат Сокслета;
* емкости из темного стекла с притертыми крышками;
* емкости из темного стекла с навинчиваемыми крышками;
Стакан 7 по ГОСТ 9147;
* ступку 3. пестик 2 по ГОСТ 9147.
5.2 Для определения содержания ПХДД/ПХДФ применяют следующие реактивы:
Азот газообразный по ГОСТ 9293. марки ос. ч.;
* оксид алюминия 60. щелочной, активность Брокмана (I):
Ацетон по ГОСТ 2603. ч. д. а.;
Гелий газообразный (сжатый) высокой чистоты, марки А;
Дихлорметак с содержанием основного вещества не менее 99.9 %;
Изопропанол с содержанием основного вещества не менее 99,95 %;
* калий двухромовокислый по ГОСТ 4220, х. ч.;
Н-гексан с содержанием основного вещества не менее 96.0 %;
Метанол-яд ло ГОСТ 6995. х. ч.;
Нонан, х. ч.:
Натрий сернокислый безводный по ГОСТ 4166. х. ч.;
* кислоту серную концентрированную по ГОСТ 4204, х. ч.. плотностью 1.84 см 3 ;
Сорбент на основе кальцинированного диатомита (целит) с размером частиц от 0.02 до 0.10 мм (CAS No 68855-54*9);
Сорбент на основе графитизированного угля (уголь) с размером частиц от 0.177 до 0.246 мм (CAS № 7440-44-0);
Осушитель (земля диатомитовая (CAS N9 61790*53-2));
Силикагель марки 60 для колоночной хроматографии с размером частиц от 0.063 до 0.100 мм;
Толуол с содержанием основного вещества не менее 99.95 %.
5.3 Стандартные растворы и градуировочные стандарты;
5.3.1 Суррогатные изотопно-меченые и внутренние стандарты ПХДД/ПХДФ. включающие;
* раствор смеси изотопно-меченых ло углероду 13 С 12 конгенеров ПХДД/ПХДФ в нонане (раствор LCS). с погрешностью массовой концентрации каждого конгенера не более ± 10 % (см. таблицу 1).
Таблица 1-Состав раствора LCS
Конгенер | Массовая концентрация. | Конгенер | Массовая концентрация. |
2,3.7.8-ТХДД 13 С 12 | 2.3.4,7.8-ЛеХДФ 13 С, 2 | ||
1,2.3.7.8-ПеХДД 13 С 12 | 1,2,3.4.7,8-ГкХДФ 13 С, 2 | ||
1,2.3,4,7.8-ГкХДД 1э С, 2 | 1.2,3.6.7.8-ГкХДФ 1л С 12 | ||
1.2.3.6.7.8-ГкХДД,Э С, 2 | 1.2.3.7.8.9-ГкХДФ 1а С 12 | ||
1,2.3,4,6,7.8-ГпХДД 13 С, 2 | 2.3,4.6.7,8-ГкХДФ 13 С 12 | ||
охдд,3 с, 2 | 1,2,3,4,6.7,8-ГпХДФ 13 С, 2 | ||
2,3.7,8-ТХДФ,3 С, 2 | 1,2,3.4,7.8.9-ГпХДФ 13 С, 2 | ||
1.2.3.7.8-ПеХДФ,3 C V |
Раствор смеси внутренних стандартов 1,2,3,4-ТХДД,3 С 12 и 1.2,3,7,8.9-ГкХДД,3 С 12 в нонане (раствор /SS) массовой концентрацией каждого конгенера 200 нг/см 3 , и погрешностью содержания каждого конгенера не более ± 10 %.
5.3.2 Набор градуировочных стандартов CS,-CS 5 . включающий 17 токсичных конгенеров ПХДД/ ПХДФ в нонане, с погрешностью массовой концентрации каждого конгенера не более ± 10 % (см. таб* лицу 2).
Таблица 2
2,3.7.8-ТХДД | |||||
1,2.3,7,8-ПеХДД | |||||
1,2.3,4,7.8-ГкХДЦ | |||||
1.2.3.6.7.8-ГкХДД | |||||
1,2.3,7,8.9-ГкХДД | |||||
1,2.3.4,6.7.8-ГпХДД | |||||
2,3.7,8-ТХДФ | |||||
1.2.3.7.8-ПвХДФ | |||||
2,3.4,7.8-ПеХДФ | |||||
1.2.3,4,7.8-ГкХДФ | |||||
1.2.3.6,7.8-ГкХДФ | |||||
1.2.3,7,8.9-ГкХДФ | |||||
2,3.4.6,7.8-ГкХДФ | |||||
1.2.3.4,6.7,8-ГлХДФ | |||||
1,2.3.4.7.8,9-ГлХДФ | |||||
Окончание таблицы 2
2.3.7.8-ТХДД,а С, 2 | |||||
1,2,3.7.8-ПвХДД,3 С, 2 | |||||
1.2.3.4,7,8-ГкХДД 13 С 12 | |||||
1.2.3.6.7,8-ГкХДД 13 С 12 | |||||
1.2.3.4.6.7,в-ГпХДД,а С 12 | |||||
ОХДД 13 С 12 | |||||
2.3.7.В-ТХДФ 13 С 12 | |||||
1.2.3.7.8-ПвХДФ 13 С 12 | |||||
2.3,4.7,8-ПвХДФ 13 С,2 | |||||
1.2,3.4.7.8-ГкХДФ,3 С,2 | |||||
1.2.3.6.7,8-ГкХДФ,а С,2 | |||||
1.2.3.7,8.9-ГкХДФ 13 С,2 | |||||
2.3,4.6.7,8-ГкХДФ,а С,2 | |||||
1.2.3.4.6.7,в-ГпХДФ 13 С 12 | |||||
1.2.3.4,7.8.9-ГпХДФ 13 С 12 | |||||
1.2.3,4-ТХДД,3 С,2 | |||||
1.2,3.7.8.9-ГкХДД 13 С 12 |
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также вспомогательного оборудования, реактивов и материалов по качеству не ниже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и материалов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов следует использовать отдельные сушильные шкафы.
6.1.2 Стеклянную лабораторную посуду очищают хромовой смесью с последующей последовательной промывкой дистиллированной водой, затем сушат в сушильном шкафу при температуре от 105 до 110 *С.
Для приготовления хромовой смеси в фарфоровый стакан вместимостью 1000 см 3 помещают 50 г двухромовокислого калия и осторожно приливают по частям, тщательно перемешивая. 1 дм 3 концентрированной серной кислоты.
Хромовую смесь хранят в герметически закрытой стеклянной емкости.
6.1.3 Высушенную посуду ополаскивают органическими растворителями: толуолом (однократно), ацетоном (дважды). Затем проводят окончательную сушку посуды в сушильном шкафу при температуре от 105 до 110 ’С.
Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню.
6.1.4 Стекловату промывают последовательно толуолом и ацетоном в ультразвуковой баке и затем сушат при температуре 200 "С на алюминиевой фольге в сушильном шкафу в течение 10-15ч.
Чистую вату хранят в герметически закрытой стеклянной емкости.
6.1.5 Силикагель высушивают в сушильном шкафу при температуре 200 *С в течение 10-15 ч.
Силикагель хранят в герметически закрытой стеклянной емкости не более двух недель.
6.1.6 Безводный сернокислый натрий высушивают в сушильном шкафу при температуре 200 *С в течение 10-15 ч. охлаждают в эксикаторе.
Хранят в герметически закрытой стеклянной емкости не более 1 мес.
6.2 Подготовка сорбентов и реактивов
Каждую новую партию реактивов, сорбентов, материалов проверяют на отсутствие контаминации путем проведения холостого опыта в соответствии с процедурой анализа, оценивая результаты с учетом характеристик погрешности.
6.2.1 Подготовка сорбентов
6.2.1.1 Приготовление силикагеля, импрегкированного серной кислотой
8 конической колбе вместимостью 100 см 3 тщательно смешивают 60 г силикагеля (см. 6.1.5) и 40 г концентрированной серной кислоты (приливают осторожно небольшими порциями), затем ставят колбу в шейкер на 30 мин. Готовый импрегнированный силикагель должен представлять собой однородную массу без комков.
Хранят в герметически закрытой стеклянной емкости е эксикаторе в течение 1 мес.
6.2.1.2 Подготовка угля
Уголь промывают последовательной экстракцией в аппарате Сокслета толуолом в течение 24 ч. затем высушивают в сушильном шкафу при температуре 150 ’С в течение 5 ч.
Промытый уголь хранят в герметически закрытой стеклянной емкости.
6.2.1.3 Приготовление активированной смеси угля с целитом
Смешивают 9,0 г угля (см. 6.2.1.2) и 41 г целита. Активируют смесь в сушильном шкафу при тем* пературе 130 *С в течение 6 ч.
Активированную смесь угля с целитом хранят в герметически закрытой стеклянной емкости в эксикатора.
6.2.1.4 Активирование щелочного оксида алюминия
Щелочной оксид алюминия по 4 г помещают в кварцевые пробирки и активируют в муфельной печи при температуре 600 ‘С в течение 16 ч.
Активированный щелочной оксид алюминия хранят в эксикаторе не более 5 сут.
6.2.2 Подготовка и приготовление реактивов
6.2.2.1 Очистку растворителей н-гексана и дихлорметана осуществляют путем перегонки с использованием стеклянной лабораторной посуды е соответствии с правилами перегонки органических веществ. Растворители с пометкой «Для анализа пестицидов» можно использовать без дополнительной очистки.
6.2.2.2 Приготовление смеси дихлорметан-н-гексан в объемном соотношении 5:95
В мерной колбе вместимостью 100 см 3 смешивают 5 см 3 дихлорметана и 95 см 3 н-гексана.
6.2.2.3 Приготовление смеси дихлорметан«н*гексан в объемном соотношении 60:40
6 мерной колбе вместимостью 100 см 3 смешивают 60 см 3 дихлорметана и 40 см 3 н-гексана.
6.2.2.4 Приготовление смеси дихлорметан-н-гексан в объемном соотношении 1:1
8 мерной колбе вместимостью 100 см 3 смешивают равные объемы н-гексана и дихлорметана.
6.2.2.5 Приготовление смеси дихлорметан-н-гексан в объемном соотношении 25:75
8 мерной колбе вместимостью 100 см 3 смешивают 75 см 3 н-гексана и 25 см 3 дихлорметана.
6.2.2.6 Приготовление смеси дихлорметан-метанол-толуол в объемном соотношении 15:4:1
8 мерной колбе вместимостью 100 см 3 смешивают 75 см 3 дихлорметана. 20 см 3 метанола и 5 см 3 толуола.
6.2.2.7 Приготовление смеси н-гексан-изопроланол в объемном соотношении 1:1
8 мерной колбе вместимостью 500 см 3 смешивают равные объемы н-гексана и изолроланола.
6.2.2.8 Растворы, приготовленные по 6.2.2.2-в.2.2.7 хранят в емкостях из темного стекла с навинчиваемыми крышками не более 3 мес.
6.3 Приготовление растворов изотопно-меченых суррогатных и внутренних стандартов
6.3.1 Приготовление рабочего раствора смеси изотопно-меченых по углероду 13 С 12 конгенеров ПХДД/ЛХДФ в нонане (раствор LCS-1)
Для приготовления рабочего раствора LCS-1 в виалы последовательно вносят по 200 мм 3 раствора LCS (см. 5.3.1) и 800 мм 3 нонана. Массовые концентрации суррогатных стандартов в рабочем растворе (нг/см 3) приведены в таблице 3.
Таблица 3
ИзоюпнО"Мечеиый по углероду,5 С)2 конгенер | Массовая концентрация. | Иэотопмо-мечеиый ги>углероду,5 С 12 конгенер | Массовая концентрация. |
2.3.7,8-ТХДД 13 С,2 | 2.3.4.7.8-ПеХДФ 13 С 12 | ||
1.2,3.7.8-ПвХДД | 1.2.3,4.7.8-ГкХДФ 13 С 12 | ||
1.2.3.4,7.8-ГкХДД,3 С 12 | 1.2.3.6.7.8-ГкХДФ,3 С 12 | ||
1.2,3.6,7.8-ГкХДД,3 С 12 | 1.2.3,7.8.9-ГкХДФ 13 С 12 | ||
1.2.3.4.6.7.8-ГпХДД,3 С 12 | 2.3.4.6.7.&-ГкХДФ,3 С 12 | ||
ОХДД 13 С 12 | 1.2.3,4.6.7,8-ГпХДФ,а С 12 | ||
2,3.7.8-ТХДФ 13 С 12 | 1.2.3.4.7.8.9-ГпХДФ,а С 12 | ||
1.2.3.7.8-ПеХДФ 13 С 12 |
Виалы укупоривают навинчиваемыми крышками с прокладками и хранят при температуре от минус 15 *С до минус 25 е С не более 2 лет.
6.3.2 Приготовление рабочего раствора изотопно-меченого внутреннего стандарта (раствор ZSS-1)
Для приготовления рабочего раствора /SS-1 в виалы последовательно вносят по 50 мм 3 раствора ISS (см. 5.3.1) и 950 мм 3 нонана. Массовая концентрация 1Д.3.4-ТХДД,3 С, 2 и 1,2,3,7.8.9-ГкХДД,3 С, 2 составляет 10 нг/см 3 .
Виалы укупоривают навинчиваемыми крышками с прокладками и хранят при температуре от минус 15 *С до минус 25 “С не более 2 лет.
7 Отбор и подготовка проб
7.1 Отбор проб
7.1.1 Отбор проб мяса, субпродуктов - ло ГОСТ 7269.
7.1.2 Отбор проб мяса и печени птицы - по ГОСТ 31467.
7.1.3 Отбор проб масла из коровьего молока - ло ГОСТ 26809.2.
7.1.4 Отбор проб животных жиров - по ГОСТ 8285.
7.1.5 Отбор проб кормов, кормовых добавок - по ГОСТ 13496.0, кормовой муки животного происхождения - по ГОСТ 17681.
7.1.6 Пробы, отобранные по 7.1.1 и 7.1.2. при отсутствии возможности анализа в день отбора замораживают и хранят при температуре от минус 15 е С до минус 25 ’С до проведения анализа, но не более 2 мес.
7.2 Подготовка проб
7.2.1 Мышечную ткань предварительно очищают от грубой соединительной ткани. Мясо, субпродукты измельчают на гомогенизаторе.
Пробы кормов, кормовых добавок измельчают на лабораторной мельнице.
Пробы животных жиров, масла из коровьего молока используют без подготовки.
7.2.2 Определение массовой доли сырого жира в анализируемой пробе
Для проведения ускоренной экстракции растворителями следует учитывать массовую долю сырого жира в анализируемой пробе. Для этого растирают в фарфоровой ступке 5-10 г пробы с 15-20 г сернокислого безводного натрия до получения однородной сыпучей массы. Полученную смесь помещают в экстракционную ячейку вместимостью 33 см 3 , заполненную согласно рисунку 1.
1) Бумажный фильтр
2) Безводный сернокислый натрий - 2 г
3) Подготовленная проба {см. 7.2.2)
4} Безводный сернокислый натрий до края экстракционной ячейки 5) Бумажный фильтр
Рисунок 1 - Схема заполнения экстракционной ячейки
Заполненную ячейку помещают е экстрактор, устанавливая параметры экстракции ПХДД/ПХДФ в соответствии с таблицей 4.
Таблица 4
Полученный экстракт количественно переносят из приемного флакона экстрактора в предварительно высушенную до постоянной массы круглодонную колбу вместимостью 100 см 3 и упаривают досуха на ротационном испарителе при температуре 60 "С. Затем помещают колбу е сушильный шкаф и высушивают при температуре 105 *С до постоянной массы. Охлаждают в эксикаторе и взвешивают с погрешностью ±0,001 г.
Массовую долю сырого жира X. %, вычисляют по формуле
Х, 1М " ^ >10 °. (1)
гцо М 1 - масса колбы с экстрактом жира, высушенной до постоянной массы, г;
М 2 - масса пустой колбы, высушенной до постоянной массы, г;
М - масса анализируемой пробы, г.
7.3 Экстракция ПХДД/ПХДФ
7.3.1 Массу анализируемой пробы для проведения экстракции вычисляют таким образом, чтобы в ней содержалось от 3 до 5 г жира.
Для проб влажностью менее 15 % гомогенат пробы растирают в фарфоровой ступке с диатомито-вои землей до получения сыпучей смеси и используют для ускоренной экстракции.
Для проб влажностью более 15 % гомогенат пробы растирают в фарфоровой ступке с диатоми-товой землей и высушивают в микроволновой печи в течение 2-3 мин или в сушильном шкафу при температуре от 90 до 110 °C до сыпучего состояния. Высушенную пробу повторно растирают до одно родного состояния и используют для ускоренной экстракции.
Диатомитовую землю берут из расчета 2 г осушителя на 1 г гомогената пробы.
7.3.2 Подготовленную по 7.3.1 пробу (пробы животных жиров, масла из коровьего молока исполь
зуют без подготовки) помещают в экстракционную ячейку вместимостью 66 см 3 , заполненную согласно рисунку 2.
Рисунок 2 - Схема заполнения экстракционной ячейки вместимостью 66 см 3
7.3.3 Взвешивание компонентов при заполнении экстракционных ячеек проводят непосредственно в экстракционной ячейке последовательно согласно схемам их заполнения.
7.3.4 Заполненную экстракционную ячейку помещают в экстрактор, устанавливая параметры экстракции ПХДД/ПХДФ в соответствии с таблицей 5.
Таблица 5
7.3.5 Полученный экстракт количественно переносят в круглодонную колбу вместимостью 100 см 3 , упаривают на ротационном испарителе при температуре от 35 до 37 *С до объема от 1 до 2 см 3 и приводят очистку методом колоночной хроматографии по 7.4.
7.4 Очистка экстракта методом колоночной хроматографии
7.4.1 Очистка на многослойной колонке
В стеклянную колонку длиной не менее 300 мм и внутренним диаметром 10 мм (см. 5.1) помещают слой стекловаты (см. 6.1.4) и заполняют в следующем порядке:
а) 2.5 см силикагеля, импрегнированного серной кислотой (см. 6.2.1.1);
б) 0.5 см безводного сернокислого натрия:
в) 2.5 см силикагеля, импрегнированного серной кислотой:
г) 0.5 см безводного сернокислого натрия:
д) 2,5 см силикагеля, импрегнированного серной кислотой.
Каждый вносимый слой уплотняют постукиванием.
Для смачивания сорбентов через колонку пропускают 20 см 3 смеси дихлорметан-н-гексан 25:75 (см. 6.2.2.5). Под колонку подставляют чистую круглодонную колбу вместимостью 100 см 3 для сбора злюата. Затем в колонку вносят концентрированный экстракт (см. 7.3.5). Стенки колбы обмывают не менее двух раз 1 см 3 смеси дихлорметан-н-гексан 25:75 (см. 6.2.2.5) и вносят смывки в колонку после* довательно. Элюируют аналиты 25 см 3 смеси дихлорметан-н-гексан 25:75. Элюат концентрируют на роторном испарителе до объема примерно 0.1 см 3 , приливают 1 см 3 н-гексана и переходят к очистке на колонке с активированным щелочным оксидом алюминия.
7.4.2 Очистка на колонке с активированным щелочным оксидом алюминия
8 стеклянную колонку длиной не менее 150 мм и внутренним диаметром 10 мм помещают слой стекловаты (см. 6.1.4), 4 г активированного щелочного оксида алюминия (см. 6.2.1.4) и 1 см безводного сернокислого натрия. Под колонку подставляют круглодонную колбу вместимостью 100 см 3 . Колонку промывают 20 см 3 н-гексана и вносят концентрированный элюат, полученный по 7.4.1, до того как мениск растворителя достигнет сорбента, затем колонку промывают последовательно 20 см 3 н-гексана и 20 см 3 смеси дихлорметан-н-гексан 5:95 (см. 6.2.2.2) и отбрасывают собранный элюат. Затем подставляют чистую круглодонную колбу вместимостью 100 см 3 и элюируют 50 см 3 смеси дихлорметан-н-гексан 60:40 (см. 6.2.2.3). Элюат концентрируют на роторном испарителе до объема примерно 0.1 см 3 , приливают 1 см 3 н-гексана и переходят к очистке на колонке с активированной смесью угля и целита.
7.4.3 Очистка на колонке с активированной смесью угля и целита
6 стеклянную колонку длиной не менее 100 мм и внутренним диаметром 6 мм помещают слой стекловаты. 0.55 г активированной смеси угля с целитом (см. 6.2.1.3) и уплотняют тампоном из стекловаты. Подставляют круглодонную колбу вместимостью 100 см 3 и промывают колонку последовательно:
а) 5 см 3 толуола:
б) 2 см 3 смеси дихлорметан-метанол-толуол 15:4:1 (см. 6.2.2.6):
в) 1 см 3 смеси дихлорметан-н-гексан 1:1 (см. 6.2.2.4);
г) 5 см 3 н-гексана.
На промытую колонку наносят концентрированный элюат, полученный по 7.4.2, стенки колбы последовательно обмывают два раза 1 см 3 н-гексана и вносят смывки в колонку. Колонку элюируют последовательно:
а) дважды по 3 см 3 н-гексана:
б) 2 см 3 смеси дихлорметан-н-гексан 1:1 (см. 6.2.2.4);
в) 2 см 3 смеси дихлорметан-метанол-толуол 15:4:1 (см. 6.2.2.6).
Элюат отбрасывают, затем колонку переворачивают, подставляют чистую круглодонную колбу вместимостью 100 см 3 для сбора элюата и элюируют колонку 20 см 3 толуола с использованием одноканальной пипетки. Полученный элюат концентрируют на роторном испарителе до объема примерно 0.5 см 3 .
Сконцентрированный элюат количественно переносят с использованием н-гексана в виалу, предварительно добавив в нее 0,01 см 3 нонана. Осторожно упаривают в токе азота. Когда объем растворителя в виале достигнет примерно 0.1 см 3 , добавляют 0.01 см 3 раствора /SS-1 (см. 6.3.2) и продолжают упаривание до 0.01 см 3 . Полученный элюат используют для определения содержания ПХДД/ПХДФ.
7.5 Приготовление холостой пробы
Приготовление холостой пробы для контроля чистоты реактивов и посуды проводят по 7.3 и 7.4. не добавляя пробу.
8 Порядок определения ПХДД/ПХДФ
8.1 Параметры хроматографических измерений
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры, рекомендуемые изготовителем капиллярных колонок.
8.1.2 Например, для кварцевых капиллярных колонок длиной 30 или 60 м. диаметром 0.25 мм, с неподвижной полярной фазой толщиной не более 0.25 мкм устанавливают следующие параметры:
а) хроматографическая программа:
1) режим инжектора - без деления потока.
2) задержка продувки инжектора - 2 мин.
3) время сброса растворителя - 5 мин.
4) газ-носитель - гелий.
5} поток газа-носителя -1,2 см 3 /мин.
6} инжектируемый объем -1.0 мм 3 ;
б) программирование температуры:
1) начальная температура -110 °C.
2) изотерма - 3.0 мин.
3) программируемый нагрев - до температуры 200 е С со скоростью 20,0 "С/мин.
4} изотерма - 10 мин.
5) программируемый нагрев - до температуры 310 *С со скоростью 4 "С/мин,
6) температура инжектора - 280 ’С,
7) скорость потока гелия через колонку - 1.2 см 3 Умин.
8) общее время определения - 60 мин:
в) режим масс-спектрометра:
1) температура интерфейса - 280 *С.
2) температура ионного источника - 280 °C.
8.1.3 Масс-спектрометрическое измерение проводят в режиме селективного сканирования характеристических ионов аналитов. Значения отношения массы к заряду характеристических ионов (ионы, присущие только данному соединению}, используемых при измерении, приведены в таблице 6. Таблица 6
Значение отношения массы и заряду характеристических ионов т/г | ||
ТХДФ,3 С, 2 | ||
тхдд,3 С 12 | ||
ПеХДФ 1J C 12 | ||
ПеХДД 13 С 12 | ||
Окончание таблицы 6
Определяемый конгенер ПХДД/ПХДФ | Значение отношения массы к заряду харахтеристичесо<х ионое т/г | |
ГкХДФ,а С, 2 | ||
ГпХДФ,3 С,2 | ||
ГпХДД 1J C 12 | ||
8.1.4 Контроль чувствительности хромато-масс-слектрометра осуществляют введением в инжектор хроматографа 1 мм 3 градуировочного стандарта CS, (см. 5.3.2). Полученное соотношение сигнал/ шум для ТХДД должно быть не менее 10.
8.2 Градуировка хромато-масе-слектрометрической системы
8.2.1 Градуировку и расчет параметров градуировочной характеристики проводят в каждой серии анализов с использованием программного обеспечения хромато-масс-спектрометрической системы.
8.2.2 Градуировка заключается в построении зависимости площади пиков определяемых конгенеров ПХДД/ПХДФ от их концентрации. Градуировку выполняют путем анализа смесей градуировочных стандартов CS,-CS 5 (см. 5.3.2).
8.2.3 Для оценки фона (чистоты хромато-масс-спектрометрической системы) перед началом работы в инжектор хроматографа вносят 1 мм 3 нонана и записывают масс-хроматограмму. На хроматограмме не должны присутствовать пики ПХДД/ПХДФ.
8.2.4 Проводят измерения градуировочных стандартов CS,- CS 5 (см. 5.3.2) в порядке возрастания их концентраций в условиях, приведенных в 8.1.2. Каждый раствор градуировочных стандартов измеряют два раза.
Записывают масс-хроматограмму каждого раствора и с использованием программы обработки по сигналам характеристических ионов и соответствующих суррогатных изотопно-меченых стандартов определяют времена удерживания и площади пиков, соответствующие каждому определяемому конгенеру.
8.2.5 Для каждого раствора градуировочных стандартов определяют относительный фактор отклика RRF n каждого нативного (природного) конгенера ПХДД/ПХДФ относительно соответствующего изотопно-меченого конгенера, который вычисляют по формуле
вес - т ч /04
где - площадь пика конгенера ПХДД/ПХДФ в градуировочном растворе;
m js - масса соответствующего изотопно-меченого конгенера В градуировочном растворе, нг;
S, s - площадь пика соответствующего изотопно-меченого конгенера суррогатного стандарта в
растворе градуировочного стандарта; ш яг - масса конгенера ПХДД/ПХДФ в градуировочном растворе, нг.
Массу изотопно-меченого конгенера в градуировочном растворе т. нг. и массу конгенера
ПХДД/ПХДФ в градуировочном растворе т, нг. вычисляют по формуле
где С - массовая концентрация соответствующего конгенера в соответствующем градуировочном растворе, нг/см 3 ;
V - объем добавленного раствора LCS-1 или /SS-1 соответственно, см 3 .
Допустимое относительное стандартное отклонение значений относительного фактора отклика
RRF не должно превышать 20 % для всех градуировочных растворов.
8.2.6 При установке градуировочной характеристики используют линейную регрессию, которую
считают приемлемой, если рассчитанное программным обеспечением значение квадрата коэффициента корреляции для градуировочной характеристики каждого конгенера составляет не менее 0.98. Установку градуировочной характеристики проводят при каждой серии измерений заново.
8.3 Проведение измерения
8.3.1 Для определения ПХДД/ПХДФ в инжектор хроматографа вводят 1.0 мм 3 экстракта, подготовленного по 7.3, 7.4. и проводят измерения в условиях, указанных в 8.1.2. Записывают масс-хроматограммы. идентифицируют каждый конгенер ПХДД/ПХДФ и соответствующий ему изотопно-меченый конгенер суррогатного стандарта по масс-спектру и совпадению времен удерживания.
8.3.2 бремена удерживания конгенеров ПХДД/ПХДФ определяют при анализе градуировочных растворов. Для коррекции систематических сдвигов времен удерживания нативных (природных) конгенеров при обработке хроматограмм в качестве реперных пиков используют соответствующие изотопномеченые конгенеры ПХДД/ПХДФ.
8.3.3 Допустимое относительное отклонение абсолютных времен удерживания нативных (природных) конгенеров от абсолютных времен удерживания их изотопно-меченых аналогов не должно превышать 0.2 %.
8.3.4 Соотношение интенсивностей характеристических ионов на вершине пиков не отличается более чем на 15 % от значений, приведенных в таблице 7.
Таблица 7 - Допустимый интервал соотношений площадей пиков характеристических ионов
Анализ экстрактов проводят по 8.3.1. Вычисляют отношение площадей хроматографических пиков на масс-хроматограммах ионов М1 и М2, регистрируемых для каждого определяемого соединения и внутреннего стандарта, и сравнивают его со значением, приведенным в таблице 7. Это отношение 14
должно находиться в пределах допустимого интервала. Если время удерживания данного конгенера совпадает ио Временем удерживания соответствующего иэотопно<меченого внутреннего стандарта и отношение площадей пиков лежит в указанных пределах, то этот конгенер ПХДД/ПХДФ в данной пробе считают идентифицированным.
9 Обработка результатов
Массовую долю каждого конгенера ПХДД/ПХДФ в экстракте анализируемой пробы X,. нг/кг, вы-числяют по формуле
где S„ - площадь пика конгенера ПХДД/ПХДФ;
л?, - масса введенного изотопно-меченого стандарта, нг;
S suf - площадь пика соответствующего конгенера изотопно-меченого суррогатного стандарта ПХДД/ ПХДФ;
RRF n - относительный фактор отклика для каждого конгенера ПХДД/ПХДФ. вычисленный по формуле (2);
М - масса пробы, взятой для анализа, кг.
Пересчет массовой доли каждого конгенера ПХДД/ПХДФ в экстракте анализируемой пробы на жировую фракцию Х к. %, проводят по формуле
где X- - массовая доля каждого конгенера ПХДД/ПХДФ в экстракте анализируемой пробы С? нг/кг. вычисленная по формуле (4);
X - массовая доля сырого жира. %, вычисленная по формуле (1).
10 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение измерений массовой доли ПХДД/ПХДФ с расширенной неопределенностью результатов измерений при коэффициенте охвата к - 2. указанной в таблице 8.
Таблица В - Показатели правильности и прецизионности метода при проведении измерений содержания ПХДД/ПХДФ
11 Оформление результатов измерений
Результаты измерений ПХДД/ПХДФ округляют до двух значащих цифр и выражают в нанограммах на килограмм ТЭК ВОЗ" (в соответствии с ТЭФ ВОЗ для каждого конгенера, указанного в приложении А).
* Диоксиновый эквивалент токсичности (ТЭК ВОЗ) конгенеров ПХДД/ПХДФ - значение, выраженное в относительных величинах токсичности, установленных Всемирной организацией здравоохранения.
Для выражения концентрации ПХДД/ПХДФ в ТЭК ВОЗ полученные значения массовой доли конге* не ров (нг/кг) умножают на соответствующий ТЭФ ВОЗ. Результаты определения ПХДД/ПХДФ выражают суммой массовых долей конгенеров (нг/кг) ТЭК ВОЗ. округленной до двух значащих цифр.
Сумму массовых долей ПХДД/ПХДФ (нг/кг) ТЭК ВОЗ принимают за окончательный результат.
Результаты определения ПХДД/ПХДФ представляют с указанием массовой доли и границ погреш* ности (расширенной неопределенности). 1 Ю’ в млн - ’ (нг/кг). ТЭК 803
ЫХ<ТЕР;)±и оП1 , (6)
где X,- - массовая доля конгенера ПХДД/ПХДФ в пробе, нг/кг;
ТЕР, - коэффициент эквивалентной токсичности Аго конгенера ПХДД/ПХДФ;
(У О1Н - расширенная неопределенность с коэффицентом охвата двух результатов количественного
определения суммы ПХДД/ПХДФ. вычисляемая по формуле
U™*fejy i TEF,"l. (7)
где V,- - значение относительной расширенной неопределенности с коэффициентом охвата двух ре* зультатое количественного определения r-го конгенера ПХДД/ПХДФ. %;
TEF,- - коэффициент эквивалентной токсичности ^го конгенера ПХДД/ПХДФ.
12 Контроль качества результатов измерений
Контроль качества измерений обеспечивается выполнением следующих условий;
* анализ проб проводят сериями. Каждая серия включает до 10 проб, одну из которых анализи* руют дважды, и холостую пробу;
Оперативный контроль точности и правильности измерений обеспечивается анализом изотоп* но-меченых суррогатных стандартов - аналогов определяемых веществ, вводимых в каждую пробу на стадии и« подготовки.
Критерии качества анализа:
* отклонение результатов при двойном анализе пробы (предел повторяемости г. %) - не лревы* шает значения, указанного в таблице 8;
Значения величины извлечения конгенеров REC S находятся в диапазоне от 50 до 110 %. Коэффициент извлечения каждого конгенера изотопно-меченого стандарта REC S вычисляют по формуле
где S xur - площадь пика каждого конгенера изотопно-меченого суррогатного стандарта на хроматограмме анализируемой пробы;
m r - масса введенного в анализируемую пробу изотопномеченого внутреннего стандарта, нг, вычисленного по формуле (3);
S r - площадь пика каждого конгенера изотопно-меченого внутреннего стандарта на хроматограмме анализируемой пробы
где х, - фактор отклика каждого конгенера {RRF) для мо раствора градуировочных стандартов;
7 - среднее значение фактора отклика каждого конгенера; и - количество уровней градуировки;
m s - масса введенного в анализируемую пробу изотопно-меченого суррогатного стандарта, нг, вычисленного по формуле (3);
KKt- sf - относительный фактор отклика для каждого конгенера изотопно-меченого суррогатного стандарта, вычисляемый по концентрациям аналита и соответствующего внутреннего
стандарта в градуировочном растворе и полученных для них площадей хроматографических пикон
RRF « S * uf т ". (10)
где S^-площадь пика каждого конгенера иэотопно*меченого суррогатного стандарта на хроматограмме раствора градуировочного стандарта;
т,~ масса изотопно-меченого внутреннего стандарта в растворе градуировочного стандарта, нг. вычисленного по формуле (3);
S,- площадь пика каждого конгенера изотопно-меченого внутреннего стандарта на хроматограмме раствора градуировочного стандарта;
т мг- масса изотопно-меченого суррогатного стандарта в растворе градуировочного стандарта, нг. вычисленного по формуле (3);
Чувствительность прибора определяют после каждой настройки прибора путем анализа раствора градуировочного стандарта CS,. приемлемый критерий качества - соотношение сигнал:шум больше 10;1;
Линейность градуировки проверяют по результатам анализа растворов градуировочных стандартов CS,-CS 5 (см. 5.3.2). Допустимое относительное стандартное отклонение относительного фактора отклика RRF„, вычисленного по формуле (2). должно быть меньше 20 %.
При невыполнении любого из перечисленных условий принимают меры по выявлению причин и повторяют анализ проб.
Приложение А (обязательное)
Диоксиновый эквивалент токсичности (ТЭК ВОЗ) конгенеров ПХДД/ПХДФ
А.1 Диоксиновый эквивалент токсичности (ТЭК ВОЗ) конгенеров ПХДД/ПХДФ приведен в таблице А.1
Таблица А.1
Конгенер | |
Дибензодиоксины: | |
2.3.7.8-ТХДД | |
1,2.3,7,8-ПеХДД | |
1.2.3.4.7.8-ГкХДД | |
1.2.3.6.7.8-ГкХДД | |
1,2.3,7,8.9-ГкХДД | |
1,2.3.4.6.7.8-ГпХДД | |
Дибензофураны: | |
2.3,7,8-ТХДФ | |
1,2,3,7.8-ЛеХДФ | |
2,3,4,7,8-ЛеХДФ | |
1,2.3.4.7.8-ГкХДФ | |
1,2.3,6.7.8-ГкХДФ | |
2,3.4,6.7.8-ГкХДФ | |
1,2.3.7.8.9-ГкХДФ | |
1,2,3.4,6,7,8-ГпХДФ | |
1,2,3,4.7.8.9-ГпХДФ | |
УДК 637.07:614.3:006.354 МКС 65.120
Ключевые слоев: пищевые продукты, продовольственное сырье, корма, кормовые добавки, диоксины, метод определения содержания ПХДД/ПХДФ хромато-масс*спектрометрией высокого разрешения
Редактор Л.И. Нахимова Технический редактор В.Н. Прусакова Корректор Е.Р. Ароян Компьютерная еерстха Ю.В. Поповой
Слано е набор 31.08.2018. Подписано а печать 17.00.2018. Формат 80 » 84"/g Гарнитура Ариал. Уел. печ. л. 2.79. Уч.-изд. ft. 2.62.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ИД «Юриспруденция». 115419. Москва, ул. Орджоникидзе. 11. www.jurisudal.ru y-bookQmail ги
Создано в единичном исполнении ФГУП «СТЛНДАРТИНФОРМ* , 117418 Москва. Нахимовский пр-т. д. 31. и. 2. www.poslmfo.ru
Смесь конгенеров ПХДДПХДФ изотопно-меченых по углероду,а С 12 . вводимая в пробу на стадии обработки для контроля полноты извлечения и количественных расчетов.
Например, типов DB-5MS или VF-5MS. Указанные типы колонки являются рекомендуемыми. Данная информация приведена для удобства пользователей настоящего стандарта и не исключает возможности использования других типов с аналогичными характеристиками.
стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION (ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
Метод определения остаточного содержания антибиотиков тетрациклиновой группы с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Издание официальное
Стандартинформ
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 1 октября 2012 г. № 51-2012)
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2012 г. № 1424-ст межгосударственный стандарт ГОСТ 31694-2012 введен в действие в качестве национального стандарта Российской Федерации с 01 июля 2013 г.
5 Стандарт подготовлен на основе ГОСТ Р 53601-2009
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта публикуется в ежемесячно издаваемом информационном указателе «Национальные стандарты».
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра или отмены настоящего стандарта соответствующая информация будет опубликована в ежемесячно издаваемом информационном указателе «Национальные стандарты»
© Стандартинформ, 2013
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Для приготовления буферного раствора смешивают в соотношении 60:40 растворы лимонной кислоты и гидрофосфата натрия, полученные по 6.3.1 и 6.3.2, добавляют 37,2 г трилона Б, измеряют pH и, при необходимости, доводят значение pH до 4,0 ортофосфорной кислотой.
6.3.4 Приготовление растворов элюентов мобильной фазы А и Б
6.3.4.1 Для приготовления раствора элюента мобильной фазы А в мерную колбу вместимостью 1000 см 3 приливают деионизованную воду, добавляют 5 см 3 муравьиной кислоты и доводят объем до метки деионизованной водой.
6.3.4.2 Для приготовления раствора элюента мобильной фазы Б в мерную колбу вместимостью 1000 см 3 приливают метиловый спирт, добавляют 5 см 3 муравьиной кислоты и доводят объем до метки метиловым спиртом.
Срок хранения при комнатной температуре - не более 1 мес.
6.3.5 Приготовление градуировочных растворов
6.3.5.1 Приготовление градуировочных растворов тетрацикпинов
Для приготовления градуировочных растворов тетрацикпинов на весах с наибольшим пределом взвешивания 500 г взвешивают по 10 мг каждого стандартного образца по 4.1 (кроме демеклоцикпина) и переносят в мерную пробирку вместимостью 10 см 3 . Добавляют метанол, помещают в ультразвуковую баню на 1 мин и доводят полученный раствор до метки метанолом.
Массовая концентрация каждого антибиотика тетрациклиновой группы в растворе С 0 составляет 1 мг/см 3
Срок хранения раствора -3 мес при температуре минус 20 °С.
6.3.5.2 Приготовление раствора демеклоцикпина (внутреннего стандарта)
Для приготовления раствора внутреннего стандарта на весах с наибольшим пределом взвешивания 500 г взвешивают 10 мг стандарта демеклоцикпина гидрохлорида и переносят в мерную пробирку вместимостью 10 см 3 . Добавляют метанол, помещают в ультразвуковую баню на 1 мин, доводят полученный раствор до метки метанолом.
Массовая концентрация внутреннего стандарта в растворе составляет 1 мг/см 3 . Путем нескольких разбавлений доводят массовую концентрацию раствора внутреннего стандарта до значения 1 мкг/см 3 Раствор с данной концентрацией используют для внесения в исследуемые образцы.
Срок хранения раствора -3 мес при температуре минус 20 °С. 1
Перед применением растворы выдерживают при комнатной температуре, в темном месте, не менее 20 мин.
6.4 Хроматографические условия измерений
6.4.1 Хромато-масс-спектрометр включают и настраивают в соответствии с техническим руководством по его эксплуатации и устанавливают следующие хроматографические параметры:
Скорость потока элюента - 200 мм 3 /мин;
Объем вводимой пробы - 20 мм 3 .
6.4.2 Детектирование пиков проводится методом «регистрации выбранных реакций » 1) . Для каждого антибиотика тетрациклиновой группы измеряется сигнал для двух фрагментных ионов согласно таблице 1.
Более интенсивный пик (верхний в каждой строке таблицы 1) служит для определения концентрации антибиотика, второй (нижний в каждой строке таблицы 1) используется для подтверждения правильности определения. Пики ионов-фрагментов с массой 410,1 тетрациклина и доксицикпина различаются по времени их удержания в хроматографической колонке, определяемому на стадии разработки ВЭЖХ-МС/МС метода.
6.5 Построение градуировочной характеристики
6.5.1 Градуировочную кривую строят при помощи матричной градуировки. Для этого проводят обработку «чистых» проб, приготовленных и проанализированных ранее в соответствии с требованиями раздела 7, не содержащих тетра-циклинов более 1 мкг/кг для каждого из антибиотиков, в зависимости от типа исследуемой матрицы. На стадии перерастворения перед введением в хроматограф в мерную пробирку вместимостью 5 см 3 , содержащую исследуемую «чистую» пробу, добавляют градуировочный раствор тетрациклинов по 6.3.5.1 с таким расчетом, чтобы окончательные массовые концентрации находились в пределах от 1 до 1000 нг/см 3 . Затем добавляют 50 мм 3 раствора внутреннего стандарта по
6.3.5.2 и необходимое количество мобильной фазы А по 6.3.4.1, доводя объем до 1 см 3 .
6.5.2 Для получения градуировочных данных используют не менее четырех уровней концентраций матричных градуировочных растворов.
6.5.3 При построении градуировочной зависимости для количественного определения тетрациклинов анализируют матричные градуировочные растворы различных уровней концентраций в условиях, описанных в 6.2 и 6.4. Затем строят графики зависимости массовой концентрации антибиотика тетрациклиновой группы от отношения площади хроматографического пика антибиотика тетрациклиновой группы к площади пика внутреннего стандарта для каждого фрагментного иона четырех антибиотиков тетрациклиновой группы. Образец графика приведен в приложении Б.
Построение графиков может проводиться при помощи программы обработки данных ВЭЖХ-МС/МС или при помощи программы Excel (Microsoft Office).
6.5.4 Расчетные концентрации для обоих фрагментных ионов каждого антибиотика тетрациклиновой группы должны совпадать в пределах 20 %.
Градуировочная зависимость считается приемлемой, если рассчитанное значение квадрата коэффициента корреляции для градуировочной кривой каждого фрагментного иона каждого антибиотика тетрациклиновой группы не менее 0,98.
6.6 Подготовка лабораторной посуды и реактивов
6.6.1 Мойку и сушку посуды следует проводить в отдельном помещении, оборудованном приточно-вытяжной вентиляцией. Не допускается проведение подготовки посуды в данном помещении для других видов анализов. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы. 2
6.6.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.6.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105 °С до 110 °С.
7 Порядок выполнения измерений
7.1 Обработка проб органов, тканей животных, яиц, яичного порошка, молока, молочных продуктов и меда
7.1.1 Мышечную ткань предварительно очищают от грубой соединительной ткани. Яйца отделяют от скорлупы. Каждую пробу измельчают на гомогенизаторе и взвешивают по 1,0 г гомогенизированной пробы в виале на лабораторных весах с наибольшим пределом взвешивания 200 г. В виалу добавляют 50 мм 3 раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 10 см 3 экстрационного буферного раствора по 6.3.3, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 15 мин. Далее виалы с образцами помещают на предварительно охлажденную до 4 °С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин. Процедуру экстракции и центрифугирования повторяют еще один раз. Объединенные экстракты собирают в чистые виалы.
7.1.2 1,0 г меда взвешивают на лабораторных весах с наибольшим пределом взвешивания 200 г в виале вместимостью 50 см 3 . В виалу добавляют 50 мм 3 раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 20 см 3 экстрационного буферного раствора по 6.3.3, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 1 мин. Далее виалы с образцами помещают на предварительно охлажденную до 4 °С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин.
7.2 Проведение твердофазной экстракции и подготовка к хроматографированию
7.2.1 Для проведения твердофазной экстракции картридж для ТФЭ заполняют 0,5 г сорбента. Предварительно картридж кондиционируют 6 см 3 метилового спирта и уравновешивают 6 см 3 бидистиллированной воды. Затем наносят объединенный экстракт и вновь промывают 6 см 3 бидистиллированной воды. Тетра-
циклины элюируют с сорбента при помощи 6 см 3 мобильной фазы Б. Полученный элюат упаривают на нагревательном модуле в токе воздуха до 0,5 см 3 при температуре 40 °С.
7.2.2 Для перерастворения и подготовки к хроматографированию объем полученного упаренного элюата в мерной пробирке вместимостью 10 см 3 доводят до 1 см 3 при помощи мобильной фазы А и помещают на ультразвуковую баню на 1 мин. Полученный экстракт фильтруют через мембранный фильтр и используют для ВЭЖХ-МС/МС анализа.
7.3 Обработка проб молока
7.3.1 Для очистки образцов к навеске образца молока массой 1 г, помещенной в виалу, добавляют 100 мм 3 раствора внутреннего стандарта по 6.3.5.2 и оставляют для уравновешивания на 15 мин. Затем добавляют 3 см 3 ацетонитрила, закрывают крышкой и интенсивно перемешивают на встряхивателе в течение 3 мин, затем оставляют на 15 мин в горизонтальном положении для последующего уравновешивания. Далее виалу с образцом помещают на предварительно охлажденную до 4 °С центрифугу и центрифугируют при 4000 об/мин в течение 20 мин. Полученный раствор переносят в мерную пробирку вместимостью 10 см 3 и упаривают до 1 см 3 на нагревательном модуле в токе воздуха при температуре 40 °С. К полученному остатку добавляют 9 см 3 буферного раствора 6.3.3 и помещают на ультразвуковую баню.
7.3.2 Процедуру твердофазной экстракции осуществляют в соответствии с
7.2.1, а перерастворение и подготовку к хроматографированию - в соответствии с
7.4 ВЭЖХ-МС/МС анализ
7.4.1 Для определения остаточного содержания тетрациклинов и их эпиформ проводят анализ в условиях, указанных в 6.4.
7.4.2 Время удерживания антибиотиков тетрациклиновой группы определяют при анализе градуировочных растворов.
7.5 Контроль качества измерений
7.5.1 Каждая серия измерений включает в себя несколько степеней подтверждения качества измерений.
7.5.2 Для исключения контаминации образца используемыми реагентами проводят обработку «чистого образца» в соответствии с 7.1 - 7.3 в зависимости от типа исследуемой матрицы.
7.5.3 Для учета матричного эффекта при расчете остаточных содержаний антибиотиков тетрациклиновой группы используют матричную градуировку по 6.5.
7.5.4 Проводят испытание образца с обработкой пробы в соответствии 7.1 -7.3 в зависимости от типа исследуемой матрицы.
7.6 Обработка результатов хроматографического анализа
7.6.1 Расчеты содержания антибиотика тетрациклиновой группы выполняют с помощью градуировочной характеристики следующим образом. Вычисляют отношение площади пика фрагментного иона к площади внутреннего стандарта с помощью программы обработки спектров поставляемой вместе с хромато-масс-спектрометром. Затем, для найденного значения (абсциссы) находят точку на градуировочной характеристике. Ордината этой точки является искомым содержанием (приложение Б).
7.6.2 Окончательные результаты измерений содержания тетрациклинов округляют до целого значения и выражают в микрограммах на килограмм.
8 Метрологические характеристики
8.1 Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания тетрациклинов с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата к = 2, указанной в таблице 2.
Примечание - Значения относительной расширенной неопределенности, указанные в таблице 2, соответствуют границам относительной погрешности результатов измерений при Р = 0,95.
Таблица 2 - Значения относительной расширенной неопределенности измерений (при коэффициенте охвата к = 2) V, %, в диапазонах измерений содержаний антибиотиков тетрациклиновой группы, мкг/кг
|
Антибиотик тетрациклиновой |
Относительная расширенная неопределенность V n , %, при Р = 0,95 и диапазоне измерений содержания тетрациклинов, мкг/кг |
||
|
от 1,0 до 10,0 включ. |
св. 10,0 до 100,0 включ. |
св. 100,0 до 1000,0 включ. |
|
|
Тетрациклин | |||
|
Окситетрациклин | |||
|
Доксициклин | |||
|
Хлортетрациклин |
9 Оформление результатов измерений9.1 Результат анализа М с в документах, предусматривающих его использование, представляют в виде формулы м с =х П " С ±и П:С, (1)где Хп,с- среднеарифметическое значение двух параллельных измерений содержания л-го антибиотика в анализируемой пробе, мкг/кг; ±U n,c - расширенная неопределенность при коэффициенте охвата к = 2 определения содержания л-го антибиотика тетрациклиновой группы, определяемая по формуле (2), мкг/кг. 9.2 Значения расширенной неопределенности измерения рассчитывают с использованием значений относительной расширенной неопределенности при к = 2 (в соответствии с таблицей 2) по формуле где Хп,с - среднеарифметическое значение двух параллельных измерений содержания л-го антибиотика в анализируемой пробе, мкг/кг; V„ - значение относительной расширенной неопределенности содержания л-го антибиотика тетрациклиновой группы для соответствующего диапазона измерений (таблица 2). 10 Контроль качества результатов измерений10.1 Контроль полноты извлечения внутреннего стандарта тетрацик-линов 10.1.1 Контроль извлечения внутреннего стандарта тетрациклинов выполняют в ходе каждого измерения (получения результата количественного химического анализа при соблюдении требований настоящего стандарта). 10.1.2 Рассчитанные программным обеспечением значения извлечения внутренних стандартов должны находиться в диапазоне от 40 % до 130 %. Если рассчитанное значение извлечения ниже или выше указанного диапазона, то результаты измерения массовой доли тетрациклинов не принимают за окончательный результат. Проводят повторные исследования анализируемых проб. 10.2 Контроль неопределенности результатов измерений 7.3) проводить анализ градуировочных растворов в соответствии с 6.4. Результаты измерений признают удовлетворительными при выполнении следующего неравенства: Приложение Б (справочное) Отношение площади пика иона антибиотика к площади пика иона внутреннего стандарта МКС 67.050, 67.100, 67.120 МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ ПРОДУКТЫ ПИЩЕВЫЕ, ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕМетод определения остаточного содержания антибиотиков тетрацикпиновой группы с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором Food products, food raw materials. Method of determination of the antibiotic residues of tetracycline group by High Performance Liquid Chromatography - Mass Spectrometry Дата введения - 2013 - 07 - 01 1 Область примененияНастоящий стандарт устанавливает метод идентификации и количественного определения остаточного содержания антибиотиков тетрацикпиновой группы в молоке, молочной продукции, яйцах, яичном порошке, меде, органах и тканях животных с использованием высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием в диапазоне измерений от 1,0 до 1000,0 мкг/кг. 2 Нормативные ссылкиВ настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты: 3.2 Количественное определение остаточного содержания антибиотиков тетрациклиновой группы проводят методом внутреннего стандарта по сумме площадей пиков идентифицированных соединений и их эпи-форм для каждого антибиотика при помощи градуировочной кривой. 3.3 Детектирование анализируемых проб проводят в режиме регистрации выбранных реакций. 4 Средства измерений, вспомогательное оборудование, материалы, реактивы4.1 При определении содержания антибиотиков тетрациклиновой группы применяют следующие средства измерений, вспомогательное оборудование и материалы: Масс-спектрометр с диапазоном измерения от 100 до 500 атомных единиц массы (а.е.м.), массовым разрешением не менее 500, точностью измерения массы не ниже 0,2 а.е.м., с режимом получения и анализа фрагментных ионов (режим МС/МС); Систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем; термостата хроматографической колонки, обеспечивающего температуру нагрева до 50 °С; Компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов масс-спектрометрических измерений; Пипетки стеклянные градуированные по ГОСТ 29227 ; Колбы мерные стеклянные К-2-100-2, К-2-1000-2 по ГОСТ 1770 ; Виалы (флаконы полипропиленовые) вместимостью 15 и 50 см 4 с герметично закрывающимися пластмассовыми крышками ; Фильтры мембранные с размером пор не более 0,5 мкм ; Измельчитель-гомогенизатор лабораторный ; Встряхиватель вибрационный для пробирок орбитального типа движения с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2500 об/мин ; Центрифугу лабораторную рефрижераторную со скоростью вращения ротора не менее 10000 об/с и диапазоном температур охлаждения от 4 °С до 20 °С, с адаптерами для пробирок вместимостью 15 см 3 и микроцентрифужных пробирок вместимостью 1,5 см 3 ; Модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования 40 °С ; Баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм 3 ; Колонку хроматографическую обращенно-фазную длиной не менее 50 мм с диаметром частиц сорбента не более 5 мкм; Устройство вакуумное для твердофазной экстракции; Картридж для твердофазной экстракции объемом не менее 12 см 3 , заполненный обращенно-фазным сорбентом с диаметром частиц не более 50 мкм; Камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 18 °С до минус 24 °С; Холодильник бытовой с морозильной камерой, цифровым контроллером температуры и рабочим диапазоном температур от 0 °С до 5 °С. 4.2 При определении содержания антибиотиков тетрацикпиновой группы применяют следующие реактивы: Кислоту лимонную пищевую по ГОСТ 908 , высшего сорта; Метанол х.ч.; Ацетонитрил ч.д.а.; Деионизованную воду; Муравьиную кислоту ч.д.а по ГОСТ 5848 ; Натрий фосфорнокислый двузамещенный дигидрат ч.д.а по ГОСТ 245 ;ГОСТ 13867 . 5 Требования безопасности5.1 Используемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007 , при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005 . 5.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией. 5.3 Операции по приготовлению и дозированию градуировочных растворов следует проводить под тягой в вытяжном шкафу. 5.4 В связи с тем, что при работе на хромато-масс-спектрометре используется сжатый азот, следует соблюдать требования ГОСТ 12.2.085 и правил устройства и безопасной эксплуатации сосудов, работающих под давлением, действующих на территории государства, принявшего стандарт. 5.5 При выполнении измерений на хромато-масс-спектрометре следует соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019 и инструкцией по эксплуатации прибора. 5.6 К выполнению измерений методом высокоэффективной жидкостной хроматографии - масс-спектрометрии допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации аппаратуры. 6 Порядок подготовки к проведению измерений6.1 Отбор проб 6.1.1 Отбор проб проводят в соответствии с методическими указаниями по отбору проб пищевой продукции с целью лабораторного контроля качества и безопасности, утвержденными на территории государства, принявшего стандарт. 6.1.2 Отбор проб органов, тканей животных и птицы производят в соответствии с . Масса средней пробы органов, тканей животных и птицы не менее 200 г. 6.1.3 Отбор проб молока и молочных продуктов производят в соответствии с ГОСТ 3622 . Объем средней пробы молока не менее 200 см 3 , масса средней пробы образцов молочных продуктов не менее 250 г. 6.1.4 Отбор проб меда производят в соответствии с ГОСТ 19792 . Масса средней пробы меда не менее 200 г. 6.1.5 Отбор проб яиц и яичного порошка производят в соответствии с ГОСТ 31654 и ГОСТ 30364.0 . От яиц в качестве средней пробы отбирают не менее 12 шт.; масса средней пробы яичного порошка не менее 200 г. 6.2 Подготовка хромато-масс-спектрометрической системы к выполнению измерений Подготовку хромато-масс-спектрометра к работе осуществляют в соответствии с техническим руководством по эксплуатации прибора. При этом должны быть соблюдены следующие условия: Температура окружающего воздуха..............................от 20 °С до 25 °С; Атмосферное давление.............................................от 84 до 106 кПа; Напряжение в электросети.........................................(220 + 10) В; Частота тока в электросети.........................................от 49 до 51 Гц; Относительная влажность воздуха...............................от 40 % до 80 %. 6.3 Приготовление растворов 6.3.1 Приготовление раствора лимонной кислоты молярной концентрации 0,1 моль/дм 3 В мерную колбу вместимостью 1000 см 3 вносят 21 г лимонной кислоты, растворяют в деионизированной воде и доводят объем до метки этим же растворителем. Срок хранения при комнатной температуре - не более 1 мес. 6.3.2 Приготовление раствора гидрофосфата натрия молярной концентрации 0,2 моль/ дм 3 В мерную колбу вместимостью 1000 см 3 вносят 35,6 г двузамещенного фосфата натрия, растворяют в деионизированной воде и доводят объем до метки этим же растворителем. Срок хранения при комнатной температуре - не более 1 мес. 6.3.3 Приготовление буферного раствора 6 ^ «Регистрация выбранных реакций» - режим работы масс-спектрометра, при котором детектируется ионный ток только для выбранных фрагментных ионов выбранных ионов-прекурсоров. | ||
Трудовые отношения

Должностная инструкция главного инженера, должностные обязанности главного инженера, образец должностной инструкции главного инженера Должностная инструкция главного инженера рэс
Открытие бизнеса

Где можно и где нельзя работать после туберкулеза Где можно работать после
Форекс